|
| A.烧瓶内气体的颜色不变,不再加深 |
B.NO2的物质的量浓度不变 |
| C.N2O4的消耗速率与NO2的生成速率之比为1:2 | |
| D.NO2的生成速率与NO2的消耗速率相等 |
有三种短周期元素,最外层电子数之和为17,质子数之和为31。如果这三种元素中有意种是氩元素,则关于另外两种元素的说法不正确的是
| A.若其中一种是稀有气体元素,则另一种元素一定是金属元素 |
| B.若其中一种元素的单质通常情况下是气体,则另一种元素的单质通常情况下是固体 |
| C.若其中一种元素的气态氢化物是三角锥形分子,则另一元素的所有气态氢化物一定是正四面体形分子 |
| D.若其中一种元素的最高正价是+3,则另一种元素的单质通常有两种常见同素异形体 |
X、Y两种有机物的分子式不同,但均含有C、H或C、H、O,将X、Y以任意比例混合,只要物质的量之和不变,完全燃烧时的耗氧量和生成水的量也分别不变。则下列有关判断正确的是
A.X、Y分子式中氢原子数一定要相同,与碳原子数的多少无关
B.若X为甲烷,则相对分子质量最小的Y是甲醇
C.若X为甲烷,则相对分子质量最小的Y是乙酸
D.X、Y的化学式应含有相同的氢原子数,且相差n个碳原子,同时相差2n个氧原子(n为正整数)
新鲜水果、蔬菜、乳制品中富含的维生素C具有明显的抗衰老作用,但易被空气氧化。某课外小组利用碘滴定法测某橙汁中维生素C的含量,其化学方程式为: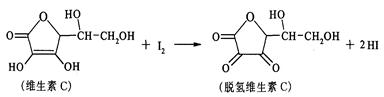
下列说法正确的是
| A.上述反应为取代反应 | B.滴定时可用淀粉溶液作指示剂 |
| C.滴定时应剧烈振荡锥形瓶 | D.脱氢维生素C的分子式为C6H6O6 |
下列4 组溶液,不用试剂也能鉴别开来的是
组溶液,不用试剂也能鉴别开来的是
①黑色粉末FeO Fe3O4 Fe CuO
②白色粉末(NH4)2SO4 NH4Cl NaSO4 NaCl
③无色溶液乙醛乙醇乙酸乙酸乙酯
④有机溶剂苯四氯化碳己烯无水乙醇
| A.③④ | B.①② | C.①②④ | D.全部 |
下列各项表达式正确的是
A.O2―的结构示意图: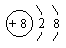 |
B.Na2S的电子式: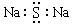 |
| C.甲醛的结构简式:CH2O | D.水的电离方程式:H2O+H2O→H3O+ +OH |