砷为第4周期ⅤA族元素,根据其在元素周期表中的位置推测,砷不可能具有的性质是( )
①砷原子比磷原子核外多一个电子层,共多8个电子 ②砷酸(H3AsO4)是一种氧化性强酸 ③砷能表现出一定的金属性 ④砷难与H2化合,砷化氢极不稳定 ⑤砷在通常状况下是固体
⑥可以有-3、+3、+5等多种化合价 ⑦As2O5对应水化物的酸性比H3PO4弱
| A.①⑥ | B.①② | C.④⑥⑦ | D.③⑤ |
两个学生在条件完 全相同的情况下测定可逆反应“A2+3B2
全相同的情况下测定可逆反应“A2+3B2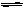 C2”的化学反应速率,甲测得
C2”的化学反应速率,甲测得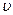 (A2) ="0.5" mol·L-1·min-1,乙测得
(A2) ="0.5" mol·L-1·min-1,乙测得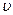 (B2)=" 1.5" mol·L-1·min-1。则这两个学生的测定结果
(B2)=" 1.5" mol·L-1·min-1。则这两个学生的测定结果
| A.都正确 | B.都错误 |
| C.甲正确,乙错误 | D.甲乙都正确或都错误 |
如图是可逆反应X2 + 3Y2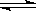 2Z2在反应过程中的反应速率
2Z2在反应过程中的反应速率 (Ʋ)与时间(t)的关系曲线,下列叙述正确的是
(Ʋ)与时间(t)的关系曲线,下列叙述正确的是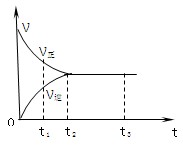
| A.t1时,只有正方向反应 |
| B.t2- t3,反应不再发生 |
| C.t2时,反应到达限度 |
| D.t2- t3,X2、Y2、Z2、的浓度之比为1:3:2 |
下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是
| 元素代号 |
L |
M |
Q |
R |
T |
||||
| 原子半径/nm |
0.160 |
0.143 |
0.089 |
0.102 |
0.074 |
||||
| 主要化合价 |
+2 |
+3 |
+2 |
+6、-2 |
-2
|
对于锌-铜-稀硫酸组成的原电池装置中,当导线中有1mol电子通过时,理论上的两极变化是:①锌片溶解了32.5g;②锌片增重了32.5g;③铜片上析出1gH2;④铜片上析出1mol H2;
| A.①和③ | B.①和④ | C.②和③ | D.②和④ |
关于化学键的各种叙述中,下列说法正确的是
| A.在离子化合物里,只存在离子键 |
| B.在共价化合物里,一定不存在离子键 |
| C.非金属元素之间构成的化合物都不是离子化合物 |
| D.由不同种元素组成的多原子分子里,一定只存在极性键 |