(本小题15分)为测定空气中CO2含量,做下述实验。
| 配0.1mol/L的标准盐酸和0.01mol/L的标准盐酸 |
→ |
用0.1mol/L的标准盐酸滴定未知Ba(OH)2溶液10mL用去盐酸19.60 mL |
→ |
用Ba(OH)2溶液吸收空气中的CO2 |
→ |
过 滤 |
→ |
取滤液20mL,用0.01mol/L的盐酸滴定用去盐酸34.8mL |
(1)为配置标准溶液,请选取必需的一组仪器 。
①托盘天平 ②容量瓶 ③滴定管 ④量筒 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒
| A.①②⑤⑥ | B.②④⑤⑥⑦ | C.②①⑥⑦ | D.②④⑤⑥ |
(2)滴定操作时,左手 ,眼睛注视 。
(3)取上述Ba(OH)2溶液10mL放入100mL容量瓶中,加水稀释至刻度,把稀释后的溶液放入密闭容器,并引入10L空气,振荡,过滤。需过滤的原因是 。
(4)由实验数据算出空气中CO2的体积分数为 。
(5)本实验中,若第一次滴定时使用的酸式滴定管未经处理,即更换溶液,进行第二次滴定,导致实验数据值(填偏高、偏低或无影响) 。
酸雨主要是大量燃烧含硫燃料放出的SO2所造成的。
(1)现有雨水样品1份,每隔一段时间测定该雨水样品的pH,所得数据如下:
| 测定时间/h |
0 |
1 |
2 |
3 |
4 |
| 雨水的pH |
4.73 |
4.62 |
4.56 |
4.55 |
4.55 |
分析数据,完成下列问题:
①雨水样品的pH变化的原因是(用化学方程式表示)________________________________。
②如果将刚取样的上述雨水和自来水混合,pH将变,原因是(用化学方程式表示)_______________________________________________________。
(2)英国的一项研究结果表明:高烟囱可以有效地降低地表面SO2的浓度。在20世纪60—70年代间,由发电厂排出的SO2增加了35%,但由于建筑高烟囱的结果,地面浓度降低了30%之多。请你从全球环境保护的角度,分析这种方法是否可取?简述其理由。
某化学兴趣小组对过量炭粉与氧化铁反应产物中气体的成分进行研究。
(1)假设该反应的气体产物全部是二氧化碳。
(2)设计方案:将一定量氧化铁在隔绝氧气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比。
(3)查阅资料:氮气不与炭、氧化铁发生反应,可用来隔绝氧气。
(4)实验:
| 操作步骤和实验现象 |
简答 |
| ①称取3.2 g氧化铁与2 g炭粉均匀混合,放入48.48 g的玻璃管中,按上图装置连接 |
①写出装置中编号仪器的名称: A__________,B__________ |
| ②加热前,先通入一定量纯净、干燥的氮气 |
②其目的是_______________ |
| ③夹紧T处弹簧夹,加热一段时间,澄清石灰水变浑浊 |
③该现象说明__________ |
| ④完全反应后,冷却至室温,称得玻璃管和固体的总质量为52.24 g |
— |
(5)数据处理:经计算,参加反应的碳元素质量为_________g,氧元素质量为____________g。
(6)结论:根据数据处理结果,得出原假设不成立,理由是_____________________________。
课题式课堂教学是研究性学习的一种重要方式,其基本教学模式为:提出课题→确定研究方案→解决问题→总结和评价。
下面是关于“CO的化学性质”的课题式课堂教学中解决问题阶段:甲同学设计的证明CO具有还原性的实验装置,如图所示。完成下列有关问题:
(1)点燃酒精灯A、B的顺序是_______。
(2)硬质管中发生反应的化学方程式为_____________________。
(3)洗气瓶中的实验现象为_______________________________。
(4)酒精灯B的作用_____________________________________。
(5)乙同学提出甲同学装置太复杂,可将酒精灯合二为一,去掉B,而将尾气导气管出口旋转到A的火焰上即可,乙同学的设计是否合理?简述理由。
要分离CO、CO2并分别得到干燥的气体,某学生设计了如图装置,其中a是铁夹,b是分液漏斗玻璃活塞。
(1)甲容器中盛_______溶液,乙容器中盛_______溶液,丙容器盛_______溶液。
(2)实验时关闭_______ (a、b),打开_______ (a、b),发生反应的化学方程式是_______,这样得到的气体是_______。
(3)当分离完一种气体后,关闭_______ (a、b),打开_______ (a,b),发生反应的化学方程式是______________,这样得到的气体是_______。
某课外活动小组实验测得某硅酸盐所含氧化物的质量分数如下表:
| 氧化物 |
CaO |
Al2O3 |
SiO2 |
H2O |
| 质量分数 |
0.142 0 |
0.260 2 |
0.459 2 |
0.137 8 |
请你通过计算,写出该硅酸盐的普通化学式和氧化物表示式。
(1)普通化学式为_____________________________________________________;
(2)氧化物表示为_____________________________________________________。
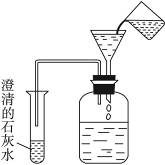
Ⅱ.如右图所示,装有萌发种子的广口瓶,过一段时间,往广口瓶里注入清水,试管里的现象是_____________________________________________________,有关的反应方程式为___________________________。