有100 mL混合气体,可能由NH3、HCl、CO2和NO组成,把混合气体通过浓H2SO4,气体体积减少30 mL,再经过Na2O2,气体又减少30 mL,最后经过水,剩余气体为20 mL(均在同温同压下测定,且不考虑水蒸气体积)。问:
(1)该混合气体由哪些气体混合而成?各占多少毫升?
(2)最后剩余20 mL是什么气体?简要说明理由。
某温度下N2O4和NO2之间建立起如下的平衡N2O4 2NO2,测得平衡混合物对空气的相对密度为2.644,求N2O4的分解率。
2NO2,测得平衡混合物对空气的相对密度为2.644,求N2O4的分解率。
在一定条件下将物质的量相等的NO和O2混合发生如下反应:2NO+O2 2NO2,2NO2
2NO2,2NO2 N2O4。所得混合气体中NO2的体积分数为40%,混合气体的平均相对分子质量。
N2O4。所得混合气体中NO2的体积分数为40%,混合气体的平均相对分子质量。
可逆反应C(s)+H2O(g) CO(g)+H2(g);△H=-Q。达到平衡后,改变温度使平衡发生移动,气体的平均相对分子质量如何变化?
CO(g)+H2(g);△H=-Q。达到平衡后,改变温度使平衡发生移动,气体的平均相对分子质量如何变化?
将70 g Na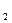 O
O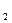 和Na
和Na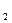 O的混合物跟98 g水充分反应后,所得氢氧化钠溶液的质量分数为50%。试通过计算推断原混合物中过氧化钠和氧化钠的质量各是多少。
O的混合物跟98 g水充分反应后,所得氢氧化钠溶液的质量分数为50%。试通过计算推断原混合物中过氧化钠和氧化钠的质量各是多少。
某种碱金属的过氧化物11 g与二氧化碳气体完全反应后,固体质量增加了2.8 g,试判断此碱金属的相对原子质量是多少,是什么金属。