在下图的实验装置中,实验开始一段时间后,对看到的现象叙述不正确的是( )
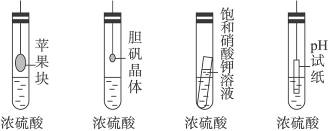
| A.苹果块会干瘪 | B.胆矾晶体表面有“白斑” |
| C.小试管内有晶体析出 | D.pH试纸变红 |
下列说法中不正确的是
| A.8NH3(g)+6NO2(g)=7N2(g)+12H2O(g) △H<O,则该反应能自发进行 |
| B.pH相等的四种溶液:a.CH3COONa b.Na2CO3 c.NaHCO3d.NaOH,则四种溶液中溶质的物质的量浓度由小到大顺序为:d<b<c<a |
| C.pH=2的一元酸和pH=12的二元强碱等体积混合:c(OH-)≤c(H+) |
| D.pH=9的CH3COONa溶液和pH=9的NH3·H2O溶液中水的电离程度相同 |
原子序数依次增大的X、Y、Z、M、W为五种短周期元素。已知Y与Z、M与W分别同周期,X与M同主族;X、Z、M的质子数之和等于Y、W的质子数之和;X与Z、M与Z都可以分别形成A2B、A2B2型的化合物;X与Y形成的气态化合物在标准状况下的密度为0.76g·L-1;Y、M、W的最高价氧化物的水化物。两两间都能发生反应。下列说法不正确的是
A.由X、M与Z形成的化合物X2Z2和M2Z2中所含的化学键类型相同
B.含有W阳离子的某种盐,可用作净水剂
C.M的单质可保存于煤油中
D.由X、Y、Z 种元素形成的某种化合物的水溶液,可能呈碱性或酸性
下列说法不正确的是
A.乙烯、乙醇均能使酸性高锰酸钾溶液褪色
B.通过乙烷的取代反应或乙烯的加成反应都可以制取纯净的氯乙烷
C.淀粉、纤维素都属于糖类,它们通式相同,但它们不互为同分异构体
下列实验装置或操作正确的是
| A.图l烧杯中通入过量的CO2出现白色沉淀,则溶液中一定含有A1O2- |
| B.图2装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、氧化性 |
| C.图3装置可以除去乙醇中的乙酸 |
| D.图4装置可以比较碳酸钠、碳酸氢钠的热稳定性 |
下列说法正确的是
| A.标况下,1.12LCl2溶于水,转移0.05NA电子 |
| B.向NH4Al(SO4)2稀溶液中逐滴加入过量Ba(OH)2溶液,离子方程式为:NH4++Al3++2SO42-+Ba2++5OH-=2BaSO4↓+AlO2-+2H2O+NH3·H2O |
| C.常温下,由水电离出的H+浓度为10-13mol·L-1的溶液中,Fe2+、Cl-、:Na+、NO3-可能大量共存 |
| D.葡萄糖(C6H12O6)溶液中:SO42-、MnO42-、K+、H+可以大量共存 |