右图是元素周期表的一部分。A、B、C、D均为短周期元素,若C原子最外层电子数是其内层电子总数的3/5,则下列说法中不正确的是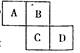
A.B元素的氢化物的沸点低于C元素的氢化物的沸点
B.B元素的两种同素异形体常温下都是气体
C.最高价氧化物对应的水化物的酸性:D>C
D.阴离子半径从大到小的排列顺序为:C>D>B
水分子间可通过一种叫“氢键”的作用(介于化学键和范德瓦耳斯力大小之间),彼此结合而形成(H2O)n,在冰中的n值为5。即每个水分子都被其他4个水分子包围形成变形四面体,如图1-11所示为(H2O)5单元,由无限个这样的四面体通过氢键相互连接成一个庞大的分子晶体,即冰。下列有关叙述正确的是()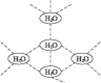
图1-11
| A.1 mol冰中有4 mol氢键 |
| B.1 mol冰中有4×5 mol氢键 |
| C.平均每个水分子只有2个氢键 |
| D.平均每个水分子只有5/4个氢键 |
共价键、离子键、分子间作用力都是粒子间的作用力,下列物质中会有以上两种作用的晶体是()
| A.SiO2 | B.Ar |
| C.NaCl | D.NaOH |
下列说法不正确的是( )
| A.金属单质的熔点一定比非金属单质高 |
| B.离子晶体中不一定含有金属元素 |
| C.在含有阳离子的晶体中,一定含有阴离子 |
| D.含有金属元素的离子不一定是阳离子 |
羟基和羧基因为在水中可以与水分子形成氢键,所以含有羟基和羧基的物质往往在水中的溶解度较大,人们把它们称为亲水基。而含烃基等非极性基团的物质在水中因极性不同,溶解度很小,所以也被称为憎水基。分子中有亲水基或亲水基比例较大的物质在水中的溶解度较大。判断下列物质中溶解度最大和最小的组合是()
①丙三醇(CH2OHCHOHCH2OH)
②C17H35COOH
③乙二醇(CH2OHCH2OH)
④C17H33COOC2H5
| A.①② | B.②④ |
| C.③④ | D.①④ |
下列叙述正确的是()
| A.同周期金属的原子半径越大,熔点越高 |
| B.同周期金属的原子半径越小,熔点越高 |
| C.同主族金属的原子半径越大,熔点越高 |
| D.同主族金属的原子半径越小,熔点越高 |