质量分数为15%的硫酸溶液18 mL,密度为1.102 g·m-1,则它的物质的量浓度最接近下列数值中的( )
| A.1.685 mol·L-1 | B.3.370 mol·L-1 |
| C.22.49 mol·L-1 | D.11.24 mol·L-1 |
用下列实验装置进行相应实验,能达到实验目的的是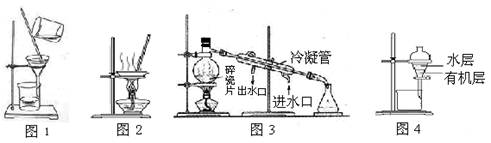
| A.用图1 所示装置除去Fe(OH)3胶体中含有的少量FeCl3杂质 |
| B.用图2 所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
| C.用图3 所示装置从海水制取蒸馏水 |
| D.用图4 所示装置分离酒精萃取碘水中的碘 |
下列关于物质分类的正确组合是
| 碱 |
酸 |
盐 |
碱性氧化物 |
酸性氧化物 |
|
| A |
纯碱 |
盐酸 |
烧碱 |
氧化铝 |
二氧化硫 |
| B |
烧碱 |
硫酸 |
食盐 |
氧化铁 |
二氧化氮 |
| C |
苛性钾 |
硬脂酸 |
小苏打 |
氧化钙 |
五氧化二磷 |
| D |
苛性钠 |
石炭酸 |
硫酸铵 |
过氧化钠 |
二氧化硅 |
化学与生活密切相关,下列说法不正确的是
| A.“地沟油”禁止食用,但可以用来制肥皂 |
| B.PM2.5作为空气质量预报的一项重要指标,它是指空气中直径小于或等于2.5μm的颗粒物,该值越高,代表空气污染程度越严重。 |
| C.静电除尘治理悬浮颗粒污染,其依据是胶体的电泳原理 |
| D.为消除碘缺乏症,卫生部规定食盐中必须加含碘物质。在食盐中所加含碘物质是KI |
将一定量的氯气通入30mL浓度为10.00mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断正确的是( )
| A.与NaOH反应的氯气一定为0.3 mol |
| B.反应后的溶液中n(Na+):n(Cl-)可能为7:3 |
| C.若反应中转移的电子为n mol,则0.15<n<0.25 |
| D.n(NaCl):n(NaClO):n(NaClO3)可能为11﹕2﹕1 |
下列说法正确的是( )
A.0.01mol/L的Na2HPO4溶液中存在如下的平衡:HPO42- H++PO43-,加水稀释,使溶液中的HPO42-、H+、PO43-的浓度均减小 H++PO43-,加水稀释,使溶液中的HPO42-、H+、PO43-的浓度均减小 |
| B.饱和NH4Cl溶液中:c(H+)+c(Cl-)=c(NH4+)+2c(NH3•H2O)+c(OH-) |
| C.常温下,0.01mol/L的 HA和BOH两种溶液,其pH值分别为3和12,将两溶液等体积混和后,所得溶液的pH≦7 |
| D.在NH4HSO3溶液中,c(NH4+)= c(SO32-)+ c(HSO3-)+ c(H2SO3) |