某混合气体可能是CO、CO2、NH3、HCl、H2和水蒸气中的一种或几种,当依次通过澄清石灰水(无浑浊现象)、氢氧化钡溶液(有浑浊现象)、浓硫酸、灼热的氧化铜(变红)和无水硫酸铜(变蓝)时,则可断定该混合气中一定有( )
| A.HCl、CO2、H2 | B.CO、H2、H2O | C.CO、H2、NH3 | D.HCl、CO、H2O |
36 g  O与80 g
O与80 g  O的物质的量之比是 ,分子中所含质子数之比是 ,所含中子数之比是 ,它们分别与Na反应时,所放出气体体积之比(同条件)是 ,质量之比是 。
O的物质的量之比是 ,分子中所含质子数之比是 ,所含中子数之比是 ,它们分别与Na反应时,所放出气体体积之比(同条件)是 ,质量之比是 。
已知碳有两种常见的同位素12C C;氧也有常见的三种同位素16O、17O、18O。由这5种粒子构成的二氧化碳分子中,其相对分子质量最多可能有( )。
C;氧也有常见的三种同位素16O、17O、18O。由这5种粒子构成的二氧化碳分子中,其相对分子质量最多可能有( )。
| A.6种 | B.10种 | C.11种 | D.12种 |
在11 g由D和18O组成的水中,含中子数为(NA表示阿伏加德罗常数)( )。
| A.NA | B.2NA | C.6NA | D.10NA |
下列说法正确的是( )。
| A.所有原子都是由质子、中子和核外电子构成的 |
| B.只要知道粒子的质子数,就一定能确定它是什么元素 |
| C.由于质量数=质子数+中子数,所以,电子是没有质量的 |
| D.分子的质子数等于该分子中各原子质子数之和 |
钛(Ti)元素的同位素有 Ti
Ti Ti
Ti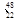 Ti
Ti Ti
Ti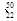 Ti,下列说法中不正确的是( )。
Ti,下列说法中不正确的是( )。
| A.上述同位素中,Ti原子核中的中子数不可能是30 |
| B.题述中包括5种钛元素,且质子数都是22 |
| C.题述中包括5种钛原子,即钛的5种核素 |
| D.钛的相对原子质量不可能为46,也不可能为50 |