氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为( )
| A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化 |
| B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道 |
| C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强 |
| D.氨气分子是极性分子而甲烷是非极性分子 |
已知某粒子的质子数,则可确定的
| A.中子数 | B.最外层电子数 | C.核电荷数 | D.相对原子质量 |
某原电池总反应是Zn+Cu2+=Zn2++Cu,该原电池组成及判断正确的是
| A |
B |
C |
D |
|
| 正极 |
Zn |
Cu |
Zn |
Cu |
| 负极 |
Cu |
Zn |
Cu |
Zn |
| 电解质溶液 |
CuCl2 |
CuCl2 |
ZnCl2 |
ZnCl2 |
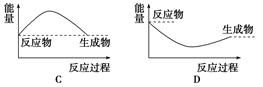
下列各图中,表示正反应是吸热反应的图是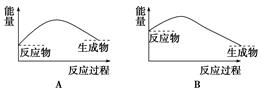
可逆反应A(g)+3B(g) 2C(g)+2D(g)在4种不同情况下反应速率分别如下,其中反应速率v最大的是
2C(g)+2D(g)在4种不同情况下反应速率分别如下,其中反应速率v最大的是
A.v(A)=0.15mol/(L·min) B.v (B)=0.6 mol/(L·min)
C.v (C)=0.3 mol/(L·min) D.v (D)=0.1 mol/(L·min)
不同的化学反应有不同的反应速率,决定化学反应速率的主要因素是
| A.温度 | B.浓度 | C.催化剂 | D.反应物的性质 |