在新研制的超导材料中,铊(Tl)是主要组成元素之一。已知铊为ⅢA族原子序数最大的金属元素,则下列关于铊元素性质的推测,不正确的是( )
| A.是银白色较软的金属 |
| B.Tl(OH)3与Al(OH) 3相似,也是两性氢氧化物 |
| C.可以形成氧化物Tl2O3 |
| D.与酸反应比铝剧烈 |
实现下列变化,一定要加入氧化剂的是
| A.HCl→Cl2 | B.Na2SO3→SO2 | C.HCl→H2 | D.HNO3→NO |
下列关于SO2的说法中,不正确的是
| A.SO2是硫及某些含硫化合物在空气中燃烧的产物 |
| B.SO2具有漂白性,可以使品红溶液褪色 |
| C.SO2与水反应生成H2SO4 |
| D.SO2既有氧化性又有还原性 |
光导纤维被认为是20世纪最伟大的发明之一。光导纤维的主要成分是
| A.Si | B.SiO2 | C.Na2SiO3 | D.SiCl4 |
世博会中国馆、主题馆等建筑使用光伏并网发电,总功率达4兆瓦,是历届世博会之最。并且使用半导体(LED)照明,节约大量能源。已知发出白光的LED 是由GaN芯片和钇铝石榴石(YAG,化学式:Y3Al5O12)芯片封装在一起做成的。下列有关叙述正确的是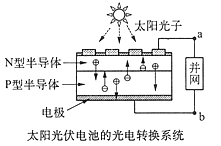
A.光伏电池是将太阳能直接转变为电能
B.图中 N 型半导体为正极, P 型半导体为负极
C.电流从 a 流向 b
D.LED 是新型有机高分子材料
下列图示与对应的叙述相符的是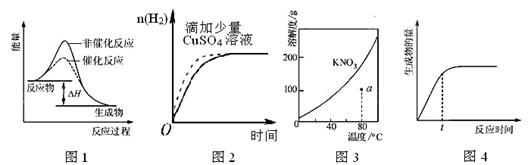
| A.图1 表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| B.图2表示常温下,等量锌粉与足量的等浓度的盐酸反应(滴加CuSO4溶液的为虚线) |
C.图3表示 KNO3 的溶解度曲线,a点所示的溶液是 80℃时 KN O3的不饱和溶液 O3的不饱和溶液 |
| D.图4表示某可逆反应生成物的量随反应时间变化的曲线, t 时反应物转化率最大 |