石英晶体的平面示意图如下图,它实际上是立体的网状结构,其中硅、氧原子数比是m
∶n,有关叙述正确的是( )
| A.m∶n=1∶2 |
| B.m∶n=2∶1 |
C.原硅酸根 的结构为[ 的结构为[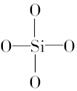 ]4-,则二聚硅酸根离子 ]4-,则二聚硅酸根离子 中的x=6 中的x=6 |
| D.六聚硅酸根[Si6O19]y-中的y=10 |
工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)=Si(s)+4HCl(g) ΔH=+Q kJ·mol-1(Q>0),某温度、压强下,将一定量的反应物通入密闭容器进行以上的反应(此条件下为可逆反应),下列叙述正确的是( )
| A.反应过程中,若增大压强能提高SiCl4的转化率 |
| B.若反应开始时SiCl4为1 mol,则达到平衡时,吸收热量为Q kJ |
| C.反应至4 min时,若HCl的浓度为0.12 mol·L-1,则H2的反应速率为0.03 mol·L-1·min-1 |
| D.当反应吸收热量为0.025 Q kJ时,生成的HCl通入100 mL 1 mol·L-1的NaOH溶液恰好反应 |
下列关于化学平衡常数的说法正确的是( )
| A.化学平衡发生移动,平衡常数必发生变化 |
| B.平衡常数发生变化,化学平衡必发生移动 |
| C.改变浓度,平衡常数一定改变 |
| D.催化剂改变达到平衡的时间,必引起平衡常数的改变 |
化合物Bilirubin在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如图所示,计算反应4~8 min间的平均反应速率和推测反应16 min时反应物的浓度,结果应是( )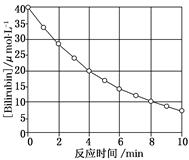
| A.2.5 μmol·L-1·min-1和2.0 μmol·L-1 |
| B.2.5 μmol·L-1·min-1和2.5 μmol·L-1 |
| C.3.0 μmol·L-1·min-1和3.0 μmol·L-1 |
| D.5.0 μmol·L-1·min-1和3.0 μmol·L-1 |
25℃和1.01×105 Pa时,反应2N2O5(g)=4NO2(g)+O2(g) ΔH=56.76 kJ·mol-1能自发进行的原因是( )
| A.是吸热反应 | B.是放热反应 |
| C.是熵减少的反应 | D.熵增大效应大于能量效应 |
用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH=-1 160 kJ·mol-1
若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移电子总数为______(阿伏加德罗常数的值用NA表示),放出的热量为______kJ。