纳米材料的表面粒子的比例极大,这是它有许多特殊性质的原因。假设某氯化钠纳米颗粒的大小和形状恰好与氯化钠晶胞的大小和形状相同(如下图所示),则这种纳米颗粒的表面粒子数与总粒子数的比值为( )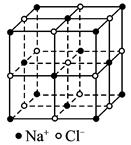
| A.7∶8 | B.13∶14 | C.25∶26 | D.26∶27 |
已知:2SO2(g)+O2(g) 2SO3(g)ΔH=-Q kJ·mol-1 (Q>0),下列说法正确的是
2SO3(g)ΔH=-Q kJ·mol-1 (Q>0),下列说法正确的是
| A.相同条件下,2 mol SO2(g)和1 mol O2(g)所具有的能量小于2 mol SO3(g)所具有的能量 |
| B.将2 mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后,放出热量为Q kJ |
| C.增大压强或升高温度,该平衡都向逆反应方向移动 |
| D.将一定量SO2(g)和O2(g)置于密闭容器中充分反应放热Q kJ,此时有2 mol SO2(g)被氧化 |
下列实验事实所得出的结论中,错误的是()
| A.向AgCl沉淀中滴入稀KI溶液白色沉淀变黄,说明AgI比AgCl更难溶 |
| B.加入盐酸,产生能使澄清石灰水变浑浊的无色气体,则试样中一定有CO32- |
| C.先加入盐酸无沉淀,再加入BaCl2溶液产生白色沉淀,则试样中一定有SO42- |
| D.盐溶液中加入NaOH微热,产生使湿润的红色石蕊试纸变蓝的气体,则一定是铵盐 |
常温下,下列各组离子在指定溶液中一定能大量共存的是()
| A.无色溶液中:K+、H+、Fe2+、NO3- |
| B.c(H+)<c(OH-)的溶液中:Na+、K+、SO42-、ClO- |
| C.含0.1mol·L-1 HCO3-的溶液中:Al3+、Ca2+、NO3-、SO42- |
| D.含0.1 mol·L-1 SCN-的溶液中:Fe3+、NH4+、NO3-、Cu2+ |
在10L密闭容器中,A、B、C三种气态物质构成可逆反应体系,其关系如图所示。下列说法错误的是()
A.0~4分钟时,A的平均反应速率为 0.01mol·L-1·min-1
B.由T1向T2变化时,V正>V逆
C.此反应的正反应为吸热反应
D.其它条件不变,加压,达新平衡时,C的体积分数增大
下列有关问题与盐的水解无关的是()
| A.NH4Cl与ZnCl2溶液可作焊接金属时的除锈剂 |
| B.用NaHCO3与Al2(SO4)3两种溶液可制成泡沫灭火剂 |
| C.常温下测得NaHSO3溶液的pH小于7 |
| D.实验室盛放Na2CO3溶液的试剂瓶不能用磨口玻璃塞 |