表3-1中给出几种氯化物的熔点和沸点。
表3-1
| |
NaCl |
MgCl2 |
AlCl3 |
SiCl4 |
| 熔点(℃) |
801 |
712 |
180 |
-68 |
| 沸点(℃) |
1 465 |
1 418 |
160 |
57 |
下列关于表中四种氯化物的说法:(1)AlCl3在加热时可升华 (2)SiCl4属于分子晶体 (3)AlCl3是典型的离子晶体。其中与表中数据一致的是( )
| A.(1)和(2) | B.只有(3) | C.(2)(3) | D.全部一致 |
下列操作正确的是
| A.用盐酸溶液清洗盛过苯酚的试管 |
| B.向放有电石的圆底烧瓶中,滴入饱和食盐水可产生乙炔气体 |
| C.将2%的NaOH溶液4~5滴,滴入2 mL10%的CuSO4溶液中制得Cu(OH)2悬浊液,加入乙醛溶液加热,用以检验醛基存在。 |
| D.将卤代烃加入到热氢氧化钠溶液中一段时间后,取上层液体,加入AgNO3液产生沉淀,则证明卤代烃中含有卤元素。 |
下列各组混合物的物质的最均为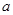 mol,组内物质按任意比例混合,完全燃烧时消耗O2的物质的量不变的是
mol,组内物质按任意比例混合,完全燃烧时消耗O2的物质的量不变的是
| A.甲烷、甲醇、甲醛 | B.乙炔、苯、1,3-二烯 |
| C.丙烯、2-丁烯、环己烷 | D.乙醇、乙烯、丙烯酸 |
A~D是中学化学实验中使用温度计的装置示意图,其中所做实验与装置不相符的是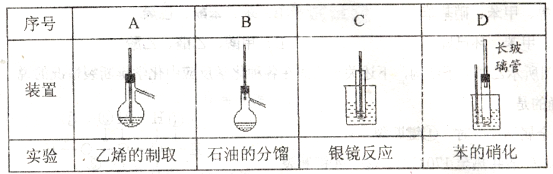
某有机物X能发生水解反应,水解产物为Y和z,同温同压下,相同质量的Y和Z的蒸气所占体积相同,化合物X可能是
| A.乙酸丙酯 | B.乙酸甲酯 | C.乙酸乙酯 | D.甲酸甲酯 |
下列反应的产物中,一定不存在同分异构体的是 