如图是某“泡腾片”的标签。将这样一粒泡腾片放入水中,药片完全溶解,同时产生大量气泡。这个过程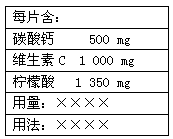
| A.溶解了500 mg的Ca2+ |
| B.释放了224 mL(标准状况)的气体 |
C.发生了反应: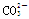 +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
| D.说明了柠檬酸的酸性比碳酸强 泡腾片 |
有一种军用烟幕弹中装有ZnO、Al粉和C2Cl6,其发烟过程中的化学反应如下:
① 3ZnO+2Al=Al2O3+3Zn;② 3Zn+C2Cl6=3ZnCl2+2C。下列有关叙述不正确的是
A.反应①是铝热反应
B.反应②是置换反应
C.C2Cl6属于有机物
D.烟幕是小液滴分散在空气中形成的
I2Cl6晶体在常温下就会“升华”,蒸气冷却可得到晶体ICl3。ICl3遇水会产生大量的腐蚀性白色烟雾,有强烈的催泪性。若生成物之一是HCl,则另一种是
| A.HIO3 | B.HIO2 | C.HIO | D.ICl |
Na2CO3、CaCO3、BaCO3、CuCO3等碳酸盐都能与相同浓度的稀硫酸反应放出CO2,其中反应最为缓慢的是
| A.BaCO3 | B.CuCO3 | C.Na2CO3 | D.CaCO3 |
铁是目前使用量最大的金属,下列有关铁及其化合物的说法正确的是
| A.铁是位于第四周期第ⅧB族的元素,是一种重要的过渡元素 |
| B.向浅绿色的Fe(NO3)2溶液中加入盐酸,溶液变黄 |
| C.14 g铁粉和7 g硫粉在空气中充分反应能生成21 g 硫化亚铁 |
| D.四氧化三铁可以看成是氧化铁和氧化亚铁组成的混合物 |