锌与不同浓度的硝酸反应,HNO3可以被还原成不同价态的产物。下列化学反应中参加反应的锌与被还原的HNO3的物质的量的关系符合图1-12(x表示被还原的HNO3的物质的量,y表示耗去Zn的物质的量)的是( )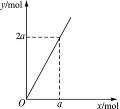
图1-12
| A.3Zn+8HNO3(稀)====3Zn(NO3)2+2NO↑+4H2O |
| B.4Zn+10HNO3(极稀) ====4Zn(NO3)2+NH4NO3+3H2O |
| C.4Zn+10HNO3(很稀) ====4Zn(NO3)2+N2O↑+5H2O |
| D.Zn+4HNO3(浓) ====Zn(NO3)2+NO2↑+2H2O |
Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如右图所示,电解总反应为: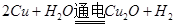 ↑。下列说法不正确的是
↑。下列说法不正确的是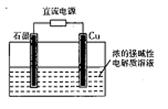
| A.石墨电极上产生氢气 |
| B.铜电极发生的电极反应为:2Cu -2e-+2OH-= Cu2O+H2O |
| C.铜电极接直流电源的正极 |
| D.当有0.1 mol电子转移时,有0.1 molCu2O生成 |
对可逆反应N2(g) +3H2(g) 2NH3(g),△H=-92.4 kJ.mol-1下列叙述正确的是
2NH3(g),△H=-92.4 kJ.mol-1下列叙述正确的是
| A.达到化学平衡时,若升高温度,则正反应速率减小,逆反应速率增大 |
| B.若单位时间内消耗x mol N2,同时生成2x mol NH3,则反应达到平衡状态 |
| C.达到平衡后,将容器体积减小为原来的一半,重新达到平衡后,c(NH3)变为原平衡时的2倍 |
| D.若达到平衡时,共放出46.2kJ热量,则有l mo1NH3(g)生成 |
对于能水解的链状有机物C4H6O2,下列说法正确的是
| A.该物质不能使溴的CC14溶液褪色 | B.该物质一定不能发生取代反应 |
| C.该物质可能的结构共有5种. | D.该物质与C2H4O2可能互为同系物 |
下列反应的离子方程式正确的是
A.Na2CO3溶液与NaHSO4溶液反应: ↑ ↑ |
B.向硫酸铵溶液中加入氢氧化钡溶液: ↓ ↓ |
| C.Fe3O4与稀硝酸反应:Fe3O4 +8H+= 2Fe3++ Fe2+ +4H2O |
| D.少量金属钠加到冷水中:Na +2H2O=Na+ +OH- +H2↑ |
下列说法正确的是
| A.欲配制1.00L 1.00mol·L-1的NaCI溶液,可将58.5g NaC1溶于1.00L水中 |
| B.0.1mol Na2O2与足量水反应,转移电子数为0.2NA |
| C.同温同压下,质量相同的SO2气体和CO2气体的体积比等16:11 |
| D.1.0L 1.0mol ·L-l的NaAlO2水溶液中含有的氧原子数大于2NA |