有甲、乙、丙三瓶等体积等物质的量浓度的NaOH溶液,若将甲蒸发掉一半水分,在乙中通入少量的CO2,丙不变,然后分别向甲、乙、丙三瓶中加入同浓度的盐酸,完全反应后所需盐酸溶液的体积是( )
| A.甲=丙>乙 | B.丙>乙>甲 |
| C.乙>甲=丙 | D.甲=乙=丙 |
已知:CO(g)+Cl2(g) COCl2(g)△H<0,当反应达到平衡时,下列措施中能提高Cl2转化率的是①升温 ②降温 ③增加CO浓度 ④加压 ⑤加催化剂 ⑥恒压通入惰性气体
COCl2(g)△H<0,当反应达到平衡时,下列措施中能提高Cl2转化率的是①升温 ②降温 ③增加CO浓度 ④加压 ⑤加催化剂 ⑥恒压通入惰性气体
| A.①④⑤ | B.②③④ | C.②④⑤ | D.③⑤⑥ |
如图所示可逆反应:mA(g)+nB(g) xC(g),△H="Q" kJ/mol,在不同温度、压强下反应物A的转化率的变化情况.下列对于反应的热效应Q和反应方程式A、B、C的化学计量数的判断中,正确的是
xC(g),△H="Q" kJ/mol,在不同温度、压强下反应物A的转化率的变化情况.下列对于反应的热效应Q和反应方程式A、B、C的化学计量数的判断中,正确的是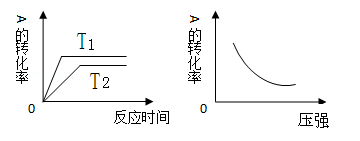
A.Q<0,m+n<x B.0,m+n>x
C.Q>0,m+n<x D.Q>0,m+n>x
反应4NH3+5O2 4NO+6H2O在一定体积的密闭容器中进行,20s后NO的物质的量浓度增加了2mol/L,则下列反应速率正确的是
4NO+6H2O在一定体积的密闭容器中进行,20s后NO的物质的量浓度增加了2mol/L,则下列反应速率正确的是
| A.v (NO)="0.02" mol•(L•s)﹣1 |
| B.v (NO)=0.2mol•(L•s)﹣1 |
| C.v (NH3)="0.1" mol•(L•s)﹣1 |
| D.v (NH3)="0.01" mol•(L•s)﹣1 |
一定温度下,在2L的密闭容器中发生如下反应:A(s)+2B(g) 2C(g)△H<0,反应过程中B、C的物质的量随时间变化关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图下列有关说法不正确的
2C(g)△H<0,反应过程中B、C的物质的量随时间变化关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图下列有关说法不正确的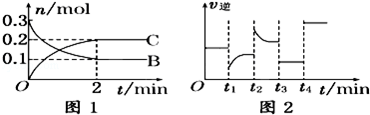
A.反应开始2分钟内,v(B)=0.05mol/(L•min)
B.t1时改变的条件可能是减小了反应物的浓度
C.t2时可能升高了温度,t3时改变的条件可能是降压,此时c(B)减小
D.T4时可能使用了催化剂
工业上处理含CO、SO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质S和CO2.已知:CO(g)+ O2(g)═CO2(g)△H=﹣283.0kJ•mol﹣1 ;S(s)+O2(g)═SO2(g)△H=﹣296.0kJ•mol﹣1此反应的热化学方程式是
O2(g)═CO2(g)△H=﹣283.0kJ•mol﹣1 ;S(s)+O2(g)═SO2(g)△H=﹣296.0kJ•mol﹣1此反应的热化学方程式是
| A.2CO(g)+SO2(g)═S(s)+2CO2(g)△H=﹣270kJ/mol |
| B.2CO(g)+SO2(g)═S(s)+2CO2(g)△H=﹣582kJ/mol |
C.CO(g)+ SO2(g)═ SO2(g)═ S(s)+CO2(g)△H=+13kJ/mol S(s)+CO2(g)△H=+13kJ/mol |
D.CO(g)+ SO2(g)═ SO2(g)═ S(s)+CO2(g)△H=+135kJ/mol S(s)+CO2(g)△H=+135kJ/mol |