离子方程式书写正确的是( )
| A.投入硫酸锌溶液中: Fe+Zn   Zn+Fe Zn+Fe |
| B.投入硫酸铜溶液中: 2Na+Cu   Cu+2Na Cu+2Na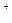 |
C.饱和Na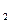 CO CO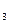 溶液中逐滴加入少量稀盐酸: 溶液中逐滴加入少量稀盐酸:CO  +2H +2H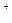  CO CO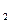 ↑+H ↑+H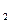 O O |
| D.投入冷水中: |
2Na+2H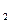 O
O 2Na
2Na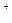 +2OH
+2OH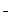 +H
+H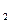 ↑
↑
下列实验现象对应的结论正确的是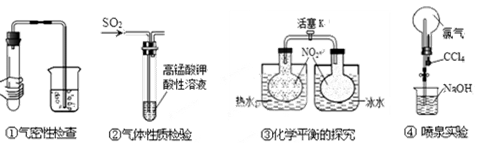
| 选项 |
现象 |
结论 |
| A |
①中导管冒气泡,手松开无现象 |
气密性良好 |
| B |
②中KMnO4溶液紫色褪去 |
SO2具有漂白性 |
| C |
③中关闭K,气体颜色在热水中比冷水深 |
NO2生成N2O4为吸热反应 |
| D |
④中烧瓶形成喷泉实验 |
Cl2易溶于CCl4 |
常温下,下列有关物质的量浓度关系正确的是
| A.等物质的量浓度的溶液中,水电离出的c(H+):HCl>CH3COOH |
| B.pH相同的溶液中:c(Na2CO3)<c(NaHCO3) |
| C.在Na2SO3溶液中:c(Na+) = 2c(SO32— ) + c(HSO3— ) + c(OH— ) |
| D.0.1mol·L—1NaHS溶液中:c(Na+) = c(HS-) |
NA为阿伏伽德罗常数,下列说法正确的是
| A.同温同压同体积的CO2和SO2所含氧原子数均为2NA |
| B.32gCu与S完全反应转移的电子数为NA(相对原子质量 Cu:64) |
| C.1L 1.0mol·L—1 NH4Cl与2L 0.5mol·L—1 NH4Cl溶液含NH4+数目相同 |
| D.25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH— 数目为0.1NA |
下列各组离子在水溶液中能大量共存的是
| A.Na+、HCO3—、SO32—、OH— | B.Al3+、H+、SiO32—、I— |
| C.Fe2+、K+、NO3—、SO42— | D.Fe3+、NH4+、ClO—、CO32— |
化学在生产和日常生活中有着重要的作用。下列有关说法不正确的是
| A.雾霾天气对人的健康造成危害,“雾”和“霾”的分散质微粒不相同 |
| B.氢氧化铁溶胶、蔗糖溶液、淀粉溶液均具有丁达尔效应 |
| C.“地沟油”经过加工处理后,可以用来制肥皂和生物柴油 |
| D.只要符合限量,“食用色素”、“亚硝酸盐”可以作为某些食品的添加剂 |