下各组物质的性质比较中,正确的是( )
A.稳定性:Na CO CO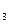 >NaHCO >NaHCO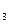 >H >H CO CO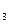 |
B.解度:Na CO CO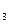 <NaHCO <NaHCO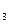 <H <H CO CO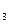 |
| C.点:Rb>K>Na>Li |
| D.原性:Rb<K<Na<Li |
下列对有关实验的说法正确的是()
| A.向盛有碘水的分液漏斗中加入无水乙醇,振荡、静置,放出有机层后再蒸馏,提取碘水中的碘 |
| B.取淀粉、稀硫酸共热后的溶液与新制Cu(OH)2反应,无红色沉淀生成,说明淀粉未水解 |
| C.用浓盐酸酸化KMnO4溶液以增强其氧化性 |
| D.为除去粗盐中的Ca2+、Mg2+、SO42-,先后加入的试剂是H2O、Ba(OH)2、Na2CO3、HCl |
下列离子方程式正确的是()
A.H2O2 + 2OH-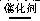 2H2O + O2↑ 2H2O + O2↑ |
B.2MnO4- + H2O2 + 6H+ = 2Mn2+ + 3O2↑+ 4H2O |
| C.2Fe3++H2S=2Fe2++S↓+2H+ | D.3ClO- + 2Fe(OH)3 = 2FeO42- + 3Cl- + H2O + 4H+ |
用NA表示阿伏加德罗常数的值。下列叙述正确的是()
| A.一定温度下,15g甲醛和乙酸的混合物中O原子数为0.5NA |
| B.常温常压下,4.6g乙醇中含有C-H键的个数为0.6NA |
| C.1molCl2和1molH2O充分反应,生成的H+离子数为NA |
| D.标准状况下,11.2L庚烷完全燃烧后生成的CO2分子数为3.5NA |
关于下列四个图像的说法中正确的是()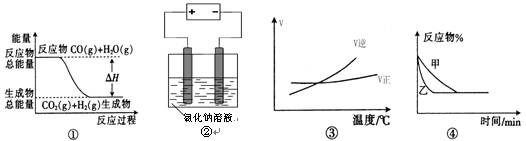


A.图①表示可逆反应“CO(g) + H2O(g) CO2(g)+H2(g)”中的ΔH大于0 CO2(g)+H2(g)”中的ΔH大于0  |
B.图②是在电解氯化钠稀溶液的电解池中,阴、阳极产生气体体积之比一定为1:1  |
C.图③可表示可逆反应“A2(g)+3B2(g) 2AB3(g)”的ΔH小于0 2AB3(g)”的ΔH小于0  |
D.图④可表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大 3C(g)+D(s)的影响,乙的压强大 |
下列比较正确的是()
①与冷水的反应速率:K>Na>Mg②热稳定性:HF>H2Se>H2S
③结合质子的能力:CH3CH2O->CH3COO->HCO3-④离子半径:Cl->O2->Al3+
| A.①④ | B.②③ | C.②④ | D.①③ |