一定条件下,在密闭容器里进行如下可逆反应:
S2Cl2(橙黄色液体)+Cl2(气) 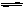 2SCl2(鲜红色液体);△H=+61.16kJ。
2SCl2(鲜红色液体);△H=+61.16kJ。
下列说法正确的是( )
| A.单位时间里生成n mol S2Cl2的同时也生成n molCl2 |
| B.达到平衡时,若升高温度,压强不变,反应混合溶液颜色变浅 |
| C.达到平衡时,单位时间里消耗n mol S2Cl2的同时也生成n molCl2 |
| D.加入氯气,平衡向正反应方向移动,氯气的转化率一定升高 |
某无色溶液中含有H+、Al3+、Mg2+三种阳离子,逐滴加入0.1moL•L﹣1NaOH溶液,消耗NaOH溶液体积(X轴)和生成沉淀(Y轴)之间的函数关系如图所示,则溶液中H+、Al3+、Mg2+三种阳离子的物质的量浓度之比为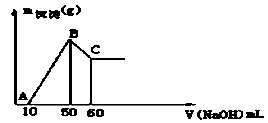
| A.1:1:1 | B.2:1:1 | C.2:2:1 | D.1:1:2 |
室温下,在0.2 mol/LAl2(SO4)3溶液中,逐滴加入1.0 mol/LNaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如下图,下列说法正确的是
| A.a点,离子方程式为:Al3+ +3OH- ==Al(OH)3↓ |
| B.a~b段,溶液pH增大,促进了氢氧化铝的碱式电离 |
| C.b~c段,加入的OH—主要用于生成Al(OH)3沉淀 |
| D.d点时,Al(OH)3沉淀开始溶解 |
有a、b、c、d 四瓶无色溶液,它们分别是Ba(OH)2溶液,NaHCO3溶液、MgCl2溶液、稀硫酸中的某一种。现各取少量溶液进行两两混合,实验现象如下表所示,表中“↓”表示生成沉淀;“↑”表示生成气体;“一”表示无明显现象。下列推理不正确的是
| A.c一定是稀硫酸 | B.d一定是MgCl2溶液 |
| C.a可能是NaHCO3溶液 | D.b一定是Ba(OH)2溶液。 |
下列实验结论正确的是
| 选项 |
实验操作 |
现象 |
结论 |
| A |
取待测液先进行焰色反应,再加足量稀盐酸,将产生气体通入品红溶液 |
火焰呈黄色,品红溶液褪色 |
原溶液一定是亚硫酸钠溶液 |
| B |
向浓醋酸溶液中加入少量碳酸钠溶液,将产生气体通入苯酚钠溶液 |
苯酚钠溶液中出现白色浑浊 |
说明酸性:醋酸>碳酸>苯酚 |
| C |
常温下向足量浓度较大的硫酸和稀硫酸中,分别加入相同质量、相同体积的铁片 |
相同时间两者产生H2速率不同[来 |
反应物的浓度越大,反应速率越快 |
| D |
相同的铝片分别与同温同体积,且c(H+)="1" mol·L¯1的盐酸、硫酸反应 |
铝与盐酸反应产生气泡较快 |
可能是Cl-对该反应起到促进作用 |
某学生鉴定甲盐的流程如图所示,下列说法正确的是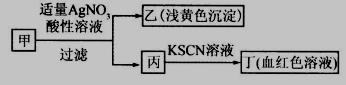
| A.如果甲中含有S2-,则乙是硫磺沉淀 |
| B.如果乙是AgCl沉淀,那么甲是FeCl3 |
| C.丙中肯定含有Fe3+,所以甲是FeBr2 |
| D.甲中含有铁元素,可能显示+2或者+3价 |