下列说法正确的是( )
| A.标准状况下,22.4 L·mol-1就是气体摩尔体积 |
| B.非标准状况下,1 mol任何气体的体积不可能为22.4 L |
| C.标准状况下,22.4 L任何气体中都含有约6.02×1023个分子 |
| D.1 mol H2和O2的混合气体在标准状况下的体积约为22.4 L |
氧化铜和氧化铁的混合物a g,加入2mol·L-1的硫酸溶液50 mL,恰好完全溶解,若将a g的该混合物在过量的CO气流中加热充分反应,冷却后剩余固体的质量为
| A.1.6a g | B.(a-1.6) g | C.(a-3.2) g | D.无法计算 |
一定物质的量的Al、Mg合金与适量的稀硫酸恰好完全反应,将反应后的溶液蒸干,所得固体(不含结晶水)质量比原固体增加了 7.2g,则该合金的物质的量可能为
| A.0. 06mol | B.0. 05mol | C.0.08mol | D.0.09mol |
关于下列图示的说法中正确的是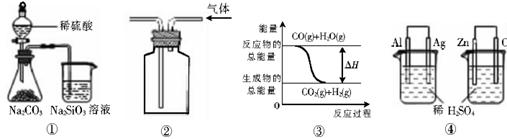
| A.用图①所示实验可比较硫、碳、硅三种元素的非金属性强弱 |
| B.用图②所示实验装置排空气法收集CO2气体 |
C.图③表示可逆反应CO(g)+H2O(g) CO2(g)+H2(g)的△H大于0 CO2(g)+H2(g)的△H大于0 |
| D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同 |
将4mol A和2mol B放入2 L密闭容器中发生反应2A(g) + B(g) 2C(g) ΔH<0。
2C(g) ΔH<0。
4 s后反应达到平衡状态,此时测得C的浓度为0.6 mol/L。下列说法正确的是
A.达到平衡状态后,若温度不变,缩小容器的体积,则A的转化率增大,平衡常数增大
B.当c(A)︰c(B)︰c(C)=2︰1︰2时,该反应即达到平衡状态
C.达到平衡状态后,若只升高温度,则C的物质的量浓度增大
D.4 s内,υ(B)=0.075 mol/(L ·s)
.已知:2H2(g)+O2(g)===2H2O(l)ΔH=-571.6 kJ·mol-1
2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l)ΔH=-1452 kJ·mol-1
H+(aq)+OH-(aq)===H2O(l)ΔH=-57.3 kJ·mol-1
下列说法正确的是
| A.H2(g)的燃烧热为571.6 kJ·mol-1 |
| B.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 |
| C.1/2H2SO4(aq)+1/2Ba(OH)2(aq)===1/2BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1 |
| D.3H2(g)+CO2(g)=CH3OH(l)+H2O(l) ΔH=+135.9 kJ·mol-1 |