6.4 g铜与60 mL浓度为8 mol·L-1的硝酸溶液充分反应,剩余溶液中含H+为n mol,此时溶液中所含NO-3的物质的量为 ( )
| A.0.31 mol | B.0.28 mol |
| C.(0.4+n) mol | D.(0.2+n) mol |
肉桂醛是一种食用香精,广泛应用于牙膏、糖果及调味品中。工业中可通过下列反应制得: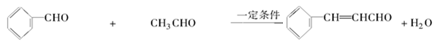 下列说法不正确的是()
下列说法不正确的是()
| A.肉桂醛的分子式为C9H8O |
| B.检验肉桂醛中是否残留有苯甲醛:加入酸性KMnO4溶液,看是否褪色 |
| C.1 mol肉桂醛完全燃烧消耗10.5 mol O2 |
| D.肉桂醛中含有的官能团:醛基、碳碳双键 |
茉莉醛具有浓郁的茉莉花香,其结构简式如图所示。下列关于茉莉醛的叙述正确的是()
| A.茉莉醛与苯甲醛互为同系物 |
| B.茉莉醛分子中最多有10个原子位于同一平面 |
| C.茉莉醛能被酸性高锰酸钾溶液、溴水等多种氧化剂氧化 |
| D.在一定条件下,1 mol茉莉醛最多能与4 mol氢气加成 |
某有机物化学式为C5H10O,它能发生银镜反应和加成反应,若将它与H2加成,所得产物的结构简式可能是()
| A.(CH3)3CCH2OH | B.(CH3CH2)2CHOH |
| C.CH3(CH2)2CH(CH3)OH | D.CH3CH2C(CH3)2OH |
今有五种有机物:
①CH2OH(CHOH)4CHO②CH3(CH2)3OH③CH2===CH—CH2OH ④CH2===CH—COOCH3
⑤CH2===CH—COOH
其中既能发生加成反应、加聚反应、酯化反应,又能发生氧化反应的是()
| A.③⑤ | B.①②⑤ | C.②④ | D.③④ |
洗涤做过银镜反应的试管可以选用的试剂是()
| A.氨水 | B.碱溶液 | C.稀硝酸 | D.酒精 |