汽油不完全燃烧的化学方程式为:
2C8H18(l)+23O2(g) 12CO2(g)+4CO(g)+18H2O(l)
12CO2(g)+4CO(g)+18H2O(l)
人体吸进CO后,CO与人体血红蛋白结合而引起中毒。如果每辆汽车满负荷行驶,每天约有28.5 g汽油不完全燃烧。现有某40万人口的中等城市,如达到中等发达国家水平,平均每10人拥有1辆汽车。请计算这些汽车满负荷行驶时,每天可产生多少千克CO。
某混合气体由一种气态烷烃和一种气态烯烃组成,在同温同压下,混合气体对氢气的相对密度为13,在标准状况下,将56.0L混合气体通入足量溴水,溴水质量增重35.0g,通过计算回答:
(1)混合气体中气态烷烃的化学式
(2)混合气体中两种气体的物质的量之比
(3)写出混合气体中气态烯烃可能的结构简式(包括顺反异构体)
一定温度下,在密闭容器中,发生反应:2NO2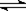 2NO+O2,经过一段时间后,测得混合气体中NO2浓度为0.06 mol·Lˉ1,O2的浓度为0.12 mol·Lˉ1,且各物质的浓度不再发生变化,求:(1) NO2的起始浓度?(2) 此时NO2的分解率?
2NO+O2,经过一段时间后,测得混合气体中NO2浓度为0.06 mol·Lˉ1,O2的浓度为0.12 mol·Lˉ1,且各物质的浓度不再发生变化,求:(1) NO2的起始浓度?(2) 此时NO2的分解率?
取100 mL的Na2CO3和Na2SO4混合溶液,加入适量Ba(OH)2溶液100 mL后,恰好完全反应,过滤、干燥后得到17.645 g白色沉淀和滤液(溶液体积为200 mL),再用过量稀硝酸处理沉淀,最后减少到5.825 g,并有气体放出。计算[第(3)问请写出计算过程]:
(1)原混合液中Na2SO4的物质的量浓度为________mol/L;
(2)产生的气体在标准状况下的体积为________L;
(3)过滤出沉淀后,计算所得滤液的物质的量浓度为多少?
19.2gCu加入到100mL一定浓度的HNO3溶液中,假定两者恰好完全反应,同时产生标准状态下8.96LNO和NO2混合气体(忽略气体的溶解及转化)。求:
(1)混合气体中NO和NO2的体积比 ?
(2)HNO3溶液的物质的量浓度?
稀硫酸与铁发生反应,生成氢气的体积为44.8 L(标准状况)。请计算反应生成氢气的质量和消耗的铁的物质的量。