(10分)实验室用燃烧法测定某种氨基酸(CxHyOzNp)的分子组成。取W g该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2。现按图所示装置进行实验。
请完成下列有关问题:
(1)实验开始时,首先要通入一段时间的氧气,其理由是______________________。
(2)装置图中需要加热的仪器有__________:(用字母填空,下同),操作时应先点燃__________处的酒精灯。
(3)A装置中发生反应的化学方程式是______________________________________。
(4)D装置的作用是______________________________________________________。
(5)读取N2的体积时,应注意:①___________;②___________。
(6)实验中测得N2的体积为V mL(已折算为标准状况)。为确定此氨基酸的分子式,还需要的有关数据有___________ (用字母填空)。
| A.生成二氧化碳气体的质量 |
| B.生成水的质量 |
| C.通入氧气的体积 |
| D.氨基酸的相对分子质量 |
氯化钠样品中含有少量的Na2SO4和Na2CO3,按下列流程进行净化。
(1)请在流程中的( )中写上合适的试剂,在[ ]中写上实验操作名称。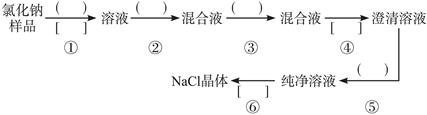
(2)写出有关反应的化学方程式:
第②步________________
第③步________________
第⑤步________________
有A、B、C三瓶失去标签的无色溶液:K2CO3、BaCl2、NaSO4。将它们分别与H2SO4作用,A产生白色沉淀,B产生无色气体,C中无明显现象。则A是________,B是________, C是________。
下列混合物的分离方法不可行的是( )
| A.互溶的液体混合物可以用分液的方法进行分离 |
| B.互不相溶的液体混合物可以用分液的方法进行分离 |
| C.沸点不同的混合物可以用蒸馏的方法进行分离 |
| D.可溶于水的固体与难溶于水的固体的混合物可用溶解、过滤的方法进行分离 |
在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可作供氧剂。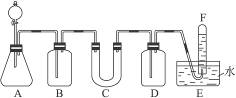
(1)A是制取CO2的装置。写出A中发生反应的化学方程式:___________________________。
(2)填写表中空格:
| 仪器 |
加入试剂 |
加入该试剂的目的 |
| B |
饱和NaHCO3溶液 |
|
| C |
||
| D |
(3)写出过氧化钠与二氧化碳反应的化学方程式:___________________________________。
(4)试管F中收集满气体后,下一步实验操作是:___________________________________。
某学生用实验方法来分析碳酸钠的纯度。该同学设计出如图②所示的实验装置(各符号代表的仪器如图①所示),其中A中盛有一定量的碳酸钠样品,分液漏斗内盛装稀硫酸,B内为碱石灰固体。他利用碱石灰的增重求出纯净的碳酸钠质量,再求纯度。重复正确操作3次,结果出现较大的偏差。
通过仔细分析,该同学重新设计了一套装置(如下图所示)(实验室可供选择的试剂和药品有锌片、浓硫酸、氢氧化钙溶液、碳酸钙固体、蒸馏水)。
完成下列问题:
(1)请分析在实验改进前,实验中出现较大偏差的原因:______________________________。
(2)在改进后的实验中,A装置分液漏斗中所盛的液体为__________,U形管内盛有。在整套装置中,A的作用是__________________________;D装置中U形管内盛有__________,D装置在整套装置中的作用是_____________________。
(3)该同学新设计的实验装置(如上图所示)是否完整?如果不完整,请画出应该补充的装置简图,并在图中标明所用药品或试剂。