A、B、C、D四种有机物的化学式均为C3H6O2,试根据下列性质确定它们的结构式:
(1)A既能跟金属钠起反应又能跟Na2CO3溶液起反应:______________________________。
(2)B既能发生银镜反应又能发生水解反应:__________________________________。
(3)C只能发生水解反应生成两种有机物:__________________________________。
(4)D既能发生银镜反应又能发生酯化反应:__________________________________。
(15分)依据事实,写出下列反应的热化学方程式。
(1)1molN2(气态)与适量H2(气态)起反应,生成 NH3(气态),放出92.2 kJ的热量;
(2)卫星发射时可用N2H4为燃料。1molN2H4(气态)在O2(气态)中燃烧,生成N2(气态)和H2O(气态),放出534kJ的热量;
(3).在101kPa时,4.0g硫粉在O2中完全燃烧生成SO2,放出37kJ的热量,S的燃烧热为______,S燃烧的热化学方程式为______。
请用化学用语表示下列名称:
(1)2个氢原子(2)硫元素
(3)硝酸中氮元素的化合价(4)氧单质(5)氢氧化钠溶液的体积
(6)氧化铁(7)4个钙离子(8)3个铵根离子。
为减少大气污染,一些城市公共汽车逐步使用CNG(压缩天然气)清洁燃料,实验测得0.16g该气体燃料,完全燃烧生成224mLCO2(标准状况)和0.36g液态水,并放出8.903KJ的热量。请写出:
CNG的化学式,其完全燃烧的热化学方程式。
Q、R、X、Y、Z五种元素的原子序数依次递增。已知: ①Z的原子序数为29,其余的均为短周期主族元素;
①Z的原子序数为29,其余的均为短周期主族元素; ②Y原子价电子(外围电子)排布msnmpn
②Y原子价电子(外围电子)排布msnmpn  ③R原子核外L层电子数为奇数;
③R原子核外L层电子数为奇数; ④Q、X原子p轨道的电子数分别为2和4。
④Q、X原子p轨道的电子数分别为2和4。 请回答下列问题:
请回答下列问题: (1)Z2+ 的核外电子排布式是,Z原子基态时简化电子排布式为。
(1)Z2+ 的核外电子排布式是,Z原子基态时简化电子排布式为。 (2)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是。
(2)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是。
| A.稳定性:甲>乙,沸点:甲>乙 | B.稳定性:甲>乙,沸点:甲<乙 |
C.稳定性:甲<乙,沸点:甲<乙 | D.稳定性:甲<乙,沸点:甲>乙 |
 (3)Q、R、Y三种元素的第一电离能数值由小到大的顺序为(用元素符号作答)。
(3)Q、R、Y三种元素的第一电离能数值由小到大的顺序为(用元素符号作答)。 (4)五种元素中,电负性最大与最小的两种非金属元素形成的化合物的化学式为。
(4)五种元素中,电负性最大与最小的两种非金属元素形成的化合物的化学式为。 (5)Q的一种氢化物相对分子质量为28,其中分子中的σ键与π键的键数之比为,该氢化物与氧气形成的燃料电池在碱性电解质中负极反应为。
(5)Q的一种氢化物相对分子质量为28,其中分子中的σ键与π键的键数之比为,该氢化物与氧气形成的燃料电池在碱性电解质中负极反应为。
1994年度诺贝尔化学奖授予为研究臭氧作出特殊贡献的化学家。O3能吸收有害紫外线,保护人类赖以生存的空间。O3分子的结构如图,呈V型,键角116.5℃。三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键——三个O原子均等地享有这4个电子。请回答: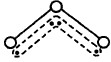
(1)臭氧与氧气的关系是。
(2)分子中某原子有1对没有跟其他原子共用的价电子叫孤对电子,那么O3分子有对孤对电子。
(3)选出下列分子与O3分子的结构最相似的的是()
| A.H2O | B.CO2 | C.SO2 | D.BeCl2 |