(10分)某有机物J(C19H20O4)不溶于水,毒性低,与聚氯乙烯、聚乙烯等树脂具有良好的相容性,是塑料工业主要增塑剂,可以用下列方法合成:
已知:
合成路线:
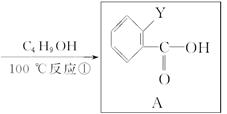



上述流程中:
(Ⅰ)反应A→B仅发生中和反应,(Ⅱ)A与浓溴水混合不产生白色沉淀。
(1)指出反应类型:反应②______________________,反应④___________。
(2)写出结构简式:Y___________,F___________。
(3)写出B+E J的化学方程式____________________________________________。
J的化学方程式____________________________________________。
(4)写出E的属于芳香烃衍生物的同分异构体的结构简式:
___________、___________、___________。
CO不仅是家用煤气的主要成分,也是重要的化工原料。下图是用某些简单有机物在低温、低压和催化剂存在下合成具有优良性能的装饰性高分子涂料、黏胶剂的基本过程。
已知CaC2与水反应的化学方程为CaC2+2H2O Ca(OH)2+HC≡CH↑。回答下列问题:
Ca(OH)2+HC≡CH↑。回答下列问题:
(1)写出G的结构简式。
(2)写出图中生成CH3OH(甲醇)的化学方程式。写出在浓硫酸作用下生成H的化学方程式。
(3)指出上述工艺的优点是什么?
现有下列短周期元素性质的数据:
| 编号 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
| 原子半径/10-10 m |
0.66 |
1.60 |
1.52 |
1.10 |
0.99 |
1.86 |
0.70 |
0.88 |
| 最高化合价 和最低化合价 |
-2 |
+2 |
+1 |
+5 -3 |
+7 -1 |
+1 |
+5 -3 |
+3 |
请确定以上8种元素在元素周期表中的位置,将元素的编号填入表中:
在一条鱼虾几乎绝迹的小河边,自上游至下游依次有甲、乙、丙、丁四座工厂,在它们排出的污水中,假设每厂只含碳酸钠、三氯化铁、氢氧化钙、盐酸中的一种。某中学环保小组对河水监测时发现:①甲处水呈乳白色;②乙处水呈红褐色;③丙处水由浑变清;④丁处产生气泡,河水仍清。回答:
(1)四厂污水中分别含(写化学式)甲___________,乙___________,丙___________,丁___________。
(2)在丁厂的下游M处取的水样中,一定含___________离子。
(3)河水中鱼虾为什么不能生存?
A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他物质已经略去):
A B
B C
C D
D
(1)若A、D的水溶液均能使湿润的蓝色石蕊试纸变红,则A、D分别为(填写化学式)。
A.___________________,D.___________________。
写出A→B转化的化学方程式:___________________________________________________。
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使蓝色的湿润石蕊试纸变红,则A为_______________。写出A→B转化的化学方程式:_______________________。
(3)若A为活泼金属元素的单质,D为强碱,焰色反应显黄色,则A是_______________,B是_______________,C是_______________。C可作为呼吸面具的填充剂,C与二氧化碳发生反应的化学方程式为:______________________________________________________。A跟水发生反应的离子方程式为:________________________________________________。
(4)若A为常见的非金属单质,则A有多种情况,请填写下表,并完成相应的化学反应方程式。(可以不填满,也可以补充)
| 编号 |
A |
B→C化学方程式 |
| ① |
||
| ② |
||
| ③ |
2005年3月29日晚7时许,在京沪高速公路淮安段发生一起交通事故:一辆载有30吨液氯的大型槽罐车与一辆货车相撞,导致槽罐车液氯大面积泄漏。由于货车司机当场死亡,肇事的槽罐车驾驶员逃逸,延误了最佳救援时机,造成公路旁三个乡镇村民的重大伤亡。接到报告后,当地政府部门紧急出动,组织施救,消防官兵迅速赶往现场。
(1)如果你当时在现场,你应该往哪里撤离?_______________(山坡上/低洼处)。
(2)如果你是当地居民,撤离时你将制备什么样的简易“防毒面具”?________________。
(3)消防官兵赶到现场后迅速将液氯罐吊入一水塘中,然后用大量碱处理。现有NaOH和Na2CO3两种物质,假如由你来选择,你选用______________________________来吸收Cl2。选择的理由是__________________________________________________________________。吸收1吨Cl2,理论要用你所选择的碱_______________吨。
(4)由于大量的氯气弥漫在空气中,消防官兵向空气中喷洒了一种挥发性的化学物质水溶液,该化学物质是
__________________________________________________________________。
(5)你对这次事故的看法以及对消防官兵处理方法的评价是__________________________。