下面是一个四肽,它可以看作是4个氨基酸缩合生成3个水分子而得。
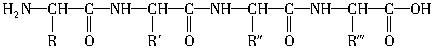 式中,R、R′、R″、
式中,R、R′、R″、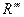 可能是相同的或不同的烃基,或有取代基的烃基,
可能是相同的或不同的烃基,或有取代基的烃基, 称为肽键。今有一个“多肽”,分子式是C55H70O19N10,已知将它彻底水解后只得到下列四种氨基酸:
称为肽键。今有一个“多肽”,分子式是C55H70O19N10,已知将它彻底水解后只得到下列四种氨基酸:


甘氨酸(C2H5NO2) 丙氨酸(C3H7NO2)
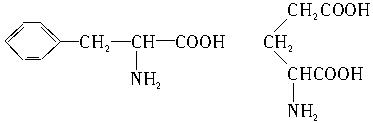
苯丙氨酸(C9H11NO2) 谷氨酸(C5H9NO4)
问:(1)这个“多肽”是几肽?
(2)该多肽水解后,有几个谷氨酸?
(3)该多肽水解后,有几个苯丙氨酸?
取100mL Na2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到29.02g白色沉淀,用过量稀硝酸处理后沉淀量减少到9.32g,并有气体放出。试计算:
(1)原混和溶液中Na2CO3和Na2SO4的物质的量浓度 (2)产生的气体在标准状况下体积。
用Pt电极电解1000mL含KNO3和Cu(NO3)2混合溶液一段时间,在两极均生成标准状况下的气体11.2L。求原混合溶液中Cu2+的物质的量浓度和电解后溶液中的H+的物质的量浓度(设电解后溶液体积不变)。
加热33.6gNaHCO3至没有气体放出时,剩余的物质是什么?计算剩余物质的质量和物质的量。
向30.0mL硫酸铜溶液中加入过量铝粉,待充分反应后,再向其中加入2.00mol/L烧碱溶液,至沉淀不再减少,消耗烧碱溶液210mL,且收集到气体0.672L(标准状况)。据此计算:
(1)加入铝粉的质量。(2)原硫酸铜溶液的物质的量浓度。
将一定质量的Al、Fe混合物加入到足量的盐酸中,充分反应后得到标准状况下的氢气8.96L;如果将等质量的该混合物加入到足量的NaOH溶液中,充分反应后得到标准状况下的氢气6.72L。
⑴.写出与碱反应涉及的化学方程式:_____________________________
⑵.混合物中Al和Fe的质量分别为________和__________
⑶.当混合物与盐酸反应时,转移电子数为_______mol;与NaOH溶液反应时转移电子数为_______mol。