下列说法正确的是( )
| A.因SiO2不溶于水,故H2SiO3不是SiO2对应的酸,或者说SiO2不是H2SiO3的酸酐 |
| B.CO2通入水玻璃(Na2SiO3溶液)可以得到原硅酸 |
| C.因为高温时SiO2与Na2CO3反应生成CO2,故硅酸的酸性比碳酸强 |
| D.SiO2的俗名叫水晶 |
下表为部分短周期元素化合价及其相应原子半径的数据。下列说法正确的是
| 元素性质 |
元素编号 |
|||||||
| A |
B |
C |
D |
E |
F |
G |
H |
|
| 原子半径(nm) |
0.102 |
0.117 |
0.074 |
0.110 |
0.071 |
0.075 |
0.077 |
0.099 |
| 最高化合价 |
+6 |
+4 |
+5 |
+5 |
+4 |
+7 |
||
| 最低化合价 |
-2 |
-4 |
-2 |
-3 |
-1 |
-3 |
-4 |
-1 |
A.C为硫元素
B.A、B是同周期元素
C.F、H的简单离子的电子层结构相同
D.元素G在周期中的位置是第二周期第Ⅳ族
下列说法正确的是
| A.实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取 |
| B.用乙醇和浓H2SO4制备乙烯时,可用水浴加热控制反应的温度 |
| C.氯离子存在时,铝表面的氧化膜易被破坏,因此含盐腌制品不宜直接放在铝制容器中 |
| D.将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性 |
下列说法不正确的是
| A.液晶态介于晶体状态和液态之间,液晶具有一定程度的晶体的有序性和液体的流动性 |
| B.常压下,0℃时冰的密度比水的密度小,水在4℃时密度最大,这些都与分子间的氢键有关 |
| C.石油裂解、煤的干馏、玉米制醇、蛋白质的变性和纳米银粒子的聚集都是化学变化 |
| D.燃料的脱硫脱氮、SO2的回收利用和NOx的催化转化都是减少酸雨产生的措施 |
下表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素的核电荷数为X元素的2倍。下列说法正确的是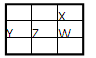
| A.X、W、Z元素的原子半径及它们的气态氢化物的热稳定性均依次递增 |
| B.Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增 |
| C.YX2晶体熔化、液态WX3气化均需克服分子间作用力 |
| D.根据元素周期律,可以推测T元素的单质具有半导体特性,T2X3具有氧化性和还原性 |
下列离子组一定能大量共存的是
| A.甲基橙呈黄色的溶液中:I-、Cl-、NO3-、Na+ |
| B.石蕊呈蓝色的溶液中:Na+、AlO2-、NO3-、HCO3- |
| C.含大量Al3+的溶液中:K+、Na+、NO3-、ClO- |
| D.含大量OH-的溶液中:CO32-、Cl-、F-、K+ |