某温度下,100 g饱和氯化钠溶液中含有氯化钠26.5 g。若向此溶液中添加3.5 g氯化钠和6.5 g水,则所得溶液的溶质质量分数是( )
| A.30% |
B. ×100% ×100% |
| C.26.5% |
D. ×100% ×100% |
在密闭容器中通入物质的量浓度均0.1mol·L-1的CH4与CO2,在一定条件下发生反应: ,测得CH4的平衡转化率与温度及压强的关系如图,下列有关说法一定正确的是
,测得CH4的平衡转化率与温度及压强的关系如图,下列有关说法一定正确的是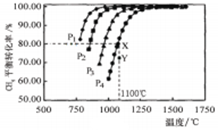
| A.上述反应的△H>0 |
| B.压强P1>P2>P3>P4 |
| C.1100℃该反应的平衡常数为64mol2·L-1 |
| D.压强为P4时,在Y点:v(正)<v(逆) |
下列根据实验操作和现象所得出的结论正确的是
| 选项 |
实验操作 |
实验现象 |
结论 |
| A |
向溴水中通入SO2气体 |
溶液褪色 |
SO2具有漂白性 |
| B |
向淀粉水解液中加入NaOH溶液至碱性,再加入新制Cu(OH)2,煮沸 |
有砖红色沉淀生成 |
淀粉已水解 |
| C |
向某钠盐X的溶液中先滴加稀盐酸,无现象,再滴加BaCl2溶液 |
出现白色沉淀 |
X一定是Na2SO4 |
| D |
BaSO4固体加入饱和Na2CO3溶液中,过滤,向滤渣中加入盐酸 |
有气体生成 |
Ksp(BaSO4)>Ksp(BaCO3) |
短周期元素X、Y、Z、W的原子序数依次增大,X是形成化合物最多的元素且X常见化合价+1和—1,Y原子最外层电子数是次外层的3倍;Z与X处于同一主族,W的原子序数是Y的2倍。下列叙述正确的是
A.原子半径的大小顺序: |
| B.元素Y的简单气态氢化物的热稳定性比W的弱 |
| C.化合物Z2Y2与X2Y反应时,Z2Y2既是氧化剂又是还原剂 |
| D.由X、Y、Z、W四种元素组成的化合物其水溶液一定显酸性 |
我国科研人员以蹄叶囊吾为原料先制得化合物I再转化为具有抗癌抑菌活性的倍半萜化合物II,有关转化如图4所示,下列有关说法不正确的是
| A.化合物I能使酸性KMnO4溶液褪色 |
| B.化合物I分子中含有5个手性碳原子 |
| C.化合物II一定条件下能发 |
| D.检验化合物II是否含化合物I可用Br2的CCl4溶液 |
下列有关说法正确的是
| A.BaSO3(s)+4C(s)=BaS(s)+4CO(g)室温下不能自发进行,说明该反应的△H>0 |
| B.纯铁和生铁在酸雨中均发生电化学腐蚀 |
C. ,其它条件不变时加入催化剂,反应速率v(SO2)和SO2转化率均增大 ,其它条件不变时加入催化剂,反应速率v(SO2)和SO2转化率均增大 |
| D.0.1mol·L-1Na2CO3溶液在35℃时碱性比25℃强,说明盐类水解反应是放热反应 |