关于浓、稀H2SO4的叙述正确的是( )
| A.浓H2SO4、稀H2SO4都难挥发 |
| B.浓H2SO4、稀H2SO4都有氧化性,故浓、稀H2SO4都是氧化性酸 |
| C.浓H2SO4、稀H2SO4在加热时都能与铜反应 |
| D.浓H2SO4、稀H2SO4在常温下都能用铁制容器储存 |
CO2气体在一定条件下可与金属镁反应,干冰在一定条件下也可以形成CO2气体,这两个变化过程中需要克服的作用分别是
| A.分子间作用力,离子键 | B.化学键,分子间作用力 |
| C.化学键,化学键 | D.分子间作用力,分子间作用力 |
已知1/2H2(g)+1/2C12(g) HCl(g);△H=-92.3kJ·mol-1,则反应2HCl(g)
HCl(g);△H=-92.3kJ·mol-1,则反应2HCl(g) H2(g)+Cl2(g)的△H1为
H2(g)+Cl2(g)的△H1为
| A.+92.3 kJ·mol-1 | B.-92.3 kJ·mol-1 |
| C.-184.6 kJ·mol-1 | D.+184.6 kJ·mol-1 |
用铁片和稀硫酸反应制氢气时,下列措施不能使氢气生成速率加快的是
| A.不用稀硫酸改用98%的浓硫酸 | B.加热 |
| C.滴加CuSO4溶液 | D.不用铁片改用铁粉 |
一定条件下,在体积一定的密闭容器中加入1 mol N2和3 mol H2发生反应:N2 + 3H2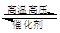 2NH3(正反应是放热反应)。下列有关说法正确的是
2NH3(正反应是放热反应)。下列有关说法正确的是
| A.达到化学反应限度时,可生成2mol NH3 |
| B.向容器中再加入N2,可以加快反应速率 |
| C.降低温度可以加快反应速率 |
| D.1mol N2和3mol H2的总能量低于2mol NH3的总能量 |
某元素最高正价与负价绝对值之差为4,该元素的离子与跟其核外电子排布相同的离子形成的化合物是
| A.K2S | B.MgO | C.MgS | D.NaF |