天然存在的金属钫(Fr)极少,它的21种已知同位素都具有放射性。它是碱金属元素中最重的元素。根据周期律知识和碱金属的性质预言其性质,其中不正确的是( )
| A.在已知元素中具有最大的原子半径 |
| B.在空气中充分燃烧时生成氧化物Fr2O |
| C.最高价氧化物对应的水化物是极强的碱 |
| D.其单质的熔点比金属钠的熔点低 |
分子组成为C4H90H并能发生催化氧化反应的有机化合物有
| A.2种 | B.4种 | C.5种 | D.3种 |
与乙烯所含碳、氢元素的质量百分含量相同,但与乙烯既不是同系物又不是同分异构体的是
A环丙烷 B乙烷 C甲烷 D CH3CH=CH2
分子式为C7H8的有机物,它能使酸性高锰酸钾溶液褪色,但不能与溴水反应,在一定条件下与H2完全加成后,其一氯代物的同分异构体有
| A.3种 | B.4种 | C.5种 | D.6种 |
对于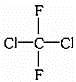 (商品名称为氟利昂—12)的叙述正确
(商品名称为氟利昂—12)的叙述正确
| A.只有一种结构 | B.有四种同分异构体 |
| C.有两种同分异构体 | D.是平面型分子 |
相同质量的下列烃,完全燃烧时,需要氧气最多的
A CH4 B C2H4 C C3H6 D C2H2