将4mol A气体和2mol B气体在2 L的容器中混合,并在一定条件下发生如下反应:2A(g)+B(g) 2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法,其中正确的是( )
2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法,其中正确的是( )
①用物质A表示的平均反应速率为0.3 mol·L-1·s-1 ②用物质B表示的平均反应速率为0.6 mol·L-1·s-1 ③2 s时物质A的转化率为70% ④2 s时物质B的浓度为0.7 mol·L-1
| A.①③ | B.①④ | C.②③ | D.③④ |
已知甲醛(HCHO)分子中的4个原子是共平面的,下列分子中所有原子不可能同时存在于同一平面的是( )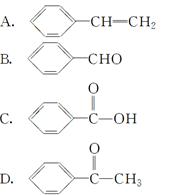
下列说法正确的是( )
| A.苯和苯乙烯是同系物 |
| B.乙醇和乙醚是同分异构体 |
| C.显酸性的有机化合物一定是羧酸 |
| D.纤维素、蛋白质、天然橡胶都是高分子化合物 |
下列化学用语使用正确的是( )
| A.葡萄糖、淀粉的最简式都是CH2O |
B.CH4的电子式是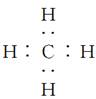 |
| C.乙醛分子的结构简式是CH3COH |
D.丙烷分子的球棍模型是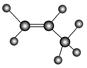 |
下列物质中,在常温常压时呈气态的是( )
| A.乙炔 | B.苯 | C.乙醇 | D.四氯化碳 |
化合物Z由如下反应得到: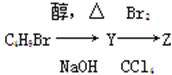 ,Z的结构简式不可能是( )
,Z的结构简式不可能是( )
| A.CH3CH2CHBrCH2Br | B.CH3CH(CH2Br)2 |
| C.CH3CHBrCHBrCH3 | D.CH2BrCBr(CH3)2 |