分子式为C5H12O的饱和一元醇的分子中含有两个—CH3,两个—CH2—,一个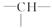 和一个—OH。它可能结构有( )
和一个—OH。它可能结构有( )
| A.2种 | B.3种 | C.4种 | D.5种 |
下列物质提纯的方法中,正确的是( )
| A.氯化铵溶液中含有少量的氯化铁,加入氢氧化钠溶液,过滤 |
| B.用NaOH溶液除去CO中的少量CO2 |
| C.将H2和O2混合气体通过炽热的CuO以除去氧气中的氢气 |
| D.H2S气体中含有水蒸气,将混合气体通过含有浓硫酸的洗气瓶 |
我们学习化学很重要的一个方面就是解决生活中的实际问题,下列家庭小实验不合理的是( )
| A.用灼烧并闻气味的方法检验真皮衣料 |
| B.用淀粉和水检验食盐中的碘元素 |
| C.用食用碱(Na2CO3)溶液洗涤餐具上的油污 |
| D.用食醋除去热水壶中的水垢 |
为达到预期的实验目的,下列操作中正确的是( )
| A.用浓NaOH溶液和蓝色石蕊试纸来检验溶液中有无NH4+ |
| B.测定某溶液的pH,先用蒸馏水润湿pH试纸,再用洁净、干燥的玻璃棒蘸取该溶液滴在试纸上,并与标准比色卡比较 |
| C.为鉴别NaNO3、Al(NO3)3和Mg(NO3)2溶液,分别向三种溶液中滴加NaOH溶液至过量 |
| D.欲分离硝酸钾和氯化钠的混合物(物质的量比为1∶1),先将样品溶解,然后加热至表面出现晶膜后冷却,过滤得硝酸钾晶体;将母液加热至大量晶体析出后,用余热蒸干,得氯化钠晶体 |
下列鉴别方法可行的是( )
| A.用氨水鉴别Al3+、Mg2+和Ag+ |
| B.用Ba(NO3)2溶液鉴别Cl-、SO42-和CO32- |
| C.菠菜中铁元素含量较高,为证明菠菜中的铁元素是+2价还是+3价,可把菠菜捣碎加水溶解,再向过滤后的滤液中加硫氰化钾溶液 |
| D.加入稀盐酸产生使澄清石灰水变浑浊的气体,则原溶液中一定含有CO32- |
用下面的方案进行某些离子的检验,其中方案设计严密的是( )
A.检验试液中的SO42-:试液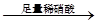 无沉淀 无沉淀 白色沉淀 白色沉淀 |
B.检验试液中的SO32-:试液 气体 气体 褪色 褪色 |
C.检验试液中的I-:试液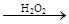 棕黄色溶液 棕黄色溶液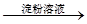 蓝色溶液 蓝色溶液 |
D.检验试液中的CO32-:试液 白色沉淀 白色沉淀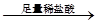 沉淀溶解 沉淀溶解 |