在海水的综合利用中,海水提溴工业是一个重要组成部分,其中一种提溴的工艺是在预先浓缩并酸化的海水中,通入足量氯气,然后使生成的溴与吸收剂SO2反应转化为氢溴酸以达到富集溴元素的目的。在有关上述工艺流程的以下化学用语中,错误的是( )
A.用电子式表示氢溴酸的形成过程为: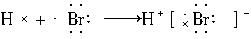 |
B.海水中Br-的电子式为: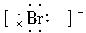 |
| C.海水中通入氯气时发生反应的离子方程式为:2Br-+Cl2====Br2+2Cl- |
D.Cl-的结构示意图为: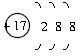 |
下列物质中全部含有极性键的是( )
| A.Br2、CO2、H2O、HBr |
| B.CO2、O2、H2S、HCl |
| C.Na2O2、S8、CO2、H2O |
| D.CO2、H2S、H2O、HI |
日常生活中用的防晒霜,如氨基苯甲酸、羟基丙酮等。它们之所以能“防晒”是( )
| A.因它们为有机物,涂用后形成了一层“保护层” |
| B.因它们挥发时吸热,降低皮肤温度 |
| C.因它们含有π键,能够有效吸收紫外线 |
| D.因它们能与皮肤形成一层“隔热层”,阻碍照射 |
下列对应不合理的是( )
| A.键能——键的能量 |
| B.键长——键的长度 |
| C.键角——键的构型 |
| D.键级——键的级别 |
下列氢化物中热稳定性最差的是( )
| A.NH3 | B.PH3 | C.AsH3 | D.SbH3 |
试指出下列物质中,键能最大的是( )
| A.F2 | B.Cl2 | C.Br2 | D.I2 |