设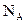 为阿伏加德罗常数的值,下列叙述中正确的是( )
为阿伏加德罗常数的值,下列叙述中正确的是( )
A.92 g NO2和N2O4混合气体中含有的分子数为2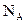 |
B.标准状况下,11.2 L SO3中含有的电子数为20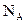 |
C.0.5 mol·L-1的Ba(OH)2溶液中OH-的数目为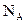 |
D.1 mol Mg与足量的O2或N2反应生成MgO或Mg3N2时,失去的电子数均为2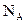 |
由丙烷、乙烯、乙炔组成的混合气体,完全燃烧后,生成CO2和H2O的物质的量相同,原混合气体中三种烃的体积比可能是( )
| A.1∶2∶1 | B.1∶2∶3 | C.2∶5∶2 | D.3∶2∶2 |
以M原子为中心形成的MX2Y2分子中,X和Y分别只以单键与M结合,下列说法正确的是( )
| A.若MX2Y2分子为平面四边形就有两种同分异构体 |
| B.若MX2Y2分子为平面四边形则无同分异构体 |
| C.若MX2Y2分子为四面体形就有两种同分异构体 |
| D.若MX2Y2分子为四面体形则无同分异构体 |
下列有机实验中不需要用温度计的是( )
| A.制乙烯 | B.制硝基苯 | C.石油分馏 | D.制溴苯 |
对下面①和②两个结构简式的说法中,正确的是( )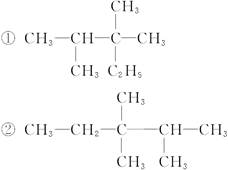
| A.①是2,3-二甲基-2-乙基丁烷 ②是3,3,4-三甲基戊烷 |
| B.①②互为同系物 |
| C.①②是同一种物质 |
| D.①②互为同分异构体 |
下列反应物的生成物为纯净物的是( )
| A.CH4和Cl2光照 |
| B.氯乙烯的加聚 |
| C.乙醇和浓H2SO4共热 |
| D.乙烯和氯化氢加成 |