有一种可溶性氯化物、溴化物、碘化物的混合物,对其进行如下测定:
①称取试样5.00 g,溶于水后加入足量AgNO3溶液,使卤离子完全沉淀为卤化银,质量为3.57 g。将该卤化银加热并通入氯气使AgBr、AgI完全转化为AgCl后,其质量变为2.87 g。
②称取试样15.00 g,溶于水后加入氯化亚钯(PdCl2)处理后,其中只有碘化物转化为PdI2沉淀,该沉淀的质量为2.16 g。
请完成下列问题:
(1)步骤①称取的试样中,所有卤原子的物质的量之和是_____________mol,该试样中碘原子的物质的量是______________mol。
(2)列式计算原混合物中溴的质量分数和氯的质量分数
在常温条件下,将0.05 mol·L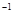 的盐酸与未知浓度的NaOH溶液以1:2的体积比混合,所得溶液的PH为2。用上述NaOH溶液与某一元弱酸HA 20.0mL反应,恰好中和时消耗NaOH溶液10.0mL,所得溶液PH为10。求:
的盐酸与未知浓度的NaOH溶液以1:2的体积比混合,所得溶液的PH为2。用上述NaOH溶液与某一元弱酸HA 20.0mL反应,恰好中和时消耗NaOH溶液10.0mL,所得溶液PH为10。求:
(1)C(NaOH)。
(2)C(HA)。
(3)盐类水解程度的大小可用“水解度(h)”来表示。对于NaA型盐的水解度(h)表示为:h =(已水解的物质的量÷原来总物质的量)×100﹪。求上述所得NaA溶液的水解度。
氮可形成多种氧化物,如NO、NO2、N2O4等,NO2和N2O4可以相互转化。
(1)对反应N2O4(g) 2NO2(g) △H>0 ,在温度为T1、 T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。T1T2(填“>”、“<”或“=”);A、C两点的速率vA vC(同上)。
2NO2(g) △H>0 ,在温度为T1、 T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。T1T2(填“>”、“<”或“=”);A、C两点的速率vA vC(同上)。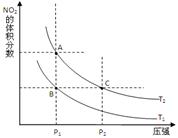
(2)在100℃时,将0.400mol的NO2气体充入2L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
| 时间(s) |
0 |
20 |
40 |
60 |
80 |
| n(NO2)/mol |
0.40 |
n1 |
0.26 |
n3 |
n4 |
| n(N2O4)/mol |
0.00 |
0.05 |
n2 |
0.08 |
0.08 |
①在上述条件下,从反应开始直至20s时,二氧化氮的平均反应速率为。
②100℃时,反应2NO2(g) N2O4(g)的平衡常数K的值为。
N2O4(g)的平衡常数K的值为。
③若在相同情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,N2O4的起始浓度是mol/L
④计算③中条件下达到平衡后混合气体的平均相对分子质量为。(结果保留小数点后一位)
Ⅰ.把0.4 mol X气体和0.6 mol Y气体混合于2 L密闭容器中,使它们发生如下反应:4X(g)+5Y(g)===nZ(g)+6W(g);2 min末已生成0.3 mol W,若测知以Z的浓度变化表示的反应速率为0.05 mol·(L·min)-1。试计算:前2 min内用X的浓度变化表示的平均反应速率为;2 min末时Y的浓度为;化学方程式中n的值是________。
Ⅱ.将64g铜与200mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为22.4L。请回答:
(1)NO的体积为L,NO2的体积为L。
(2)待产生的气体全部释放后,向溶液中加入VmL a mol·L-1的NaOH溶液,恰好使溶液中的Cu2+ 全部转化成沉淀,则原硝酸溶液的浓度为mol·L-1。(用含a、V的的式子表示)
(3)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要往其中加入25%的双氧水g。
(已知:2NO2+2NaOH=NaNO2+NaNO3+H2O; NO+NO2+2NaOH=2NaNO2+H2O)
(6分)将4 mol SO2和2 mol O2气体在2L的容器中混合,在一定条件下发生如下反应:2SO2(g)+O2 (g) 2SO3 (g)若经过2s后测得SO3的浓度为0.6 mol/ L,试计算:
2SO3 (g)若经过2s后测得SO3的浓度为0.6 mol/ L,试计算:v(O2);
SO2的转化率;
2s时的O2浓度。
(6分)在由铜片、锌片和200 mL稀硫酸组成的原电池中,若锌片只发生电化学腐蚀,当在铜片上放出3.36 L(标准状况)的H2时,硫酸恰好用完,则:
① 产生这些气体消耗的锌的质量是多少?
② 通过导线的电子的物质的量是多少?
③ 原稀硫酸的物质的量浓度是多少?