常温下,下列溶液中各组离子一定能大量共存的是
| A.使甲基橙呈红色的溶液中:Na+、AlO2-、NO3-、CO32- |
| B.由水电离产生的c(H+)=10-12mol·L-1的溶液:NH4+、SO42-、HCO3-、Cl- |
| C.c(H+)/c(OH-)= 1×1014的溶液: Ca2+、Na+、ClO-、NO3- |
D.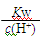 =0.1 mol·L-1的溶液:Na+、K+、CO32-、NO3- =0.1 mol·L-1的溶液:Na+、K+、CO32-、NO3- |
下列物质的系统命名中,错误的是
A.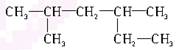 2,4-二甲基己烷 2,4-二甲基己烷 |
B.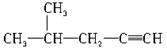 2-甲基-4-戊炔 2-甲基-4-戊炔 |
C.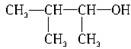 3-甲基-2-丁醇 3-甲基-2-丁醇 |
| D.CH3—CHBr—CHBr—CH3 2,3-二溴丁烷 |
分子式为C7H16的烷烃中,含有3个甲基的同分异构体的数目是
| A.2 | B.3 | C.4 | D.5 |
下列化学用语书写正确的是
A.甲烷的电子式: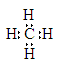 |
B.丙烯的键线式: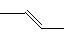 |
| C.乙烯的结构简式:CH2CH2 |
D.乙醇的结构式: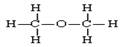 |
下列做法与可持续发展理念不符合的是
| A.加大清洁能源的开发利用,提高资源的利用率 |
| B.推广碳捕集和储存技术,逐步实现二氧化碳零排放 |
| C.加大铅酸蓄电池、含汞锌锰干电池的生产,满足消费需求 |
| D.对工业废水、生活污水净化处理,减少污染物的排放 |