非整比化合物Fe0.95O具有NaCl型晶体结构。由于n(Fe)∶n(O)<1,所以晶体存在缺陷。Fe0.95O可表示为( )
A.Fe Fe Fe O O |
B.Fe Fe Fe O O |
C.Fe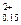 Fe Fe O O |
D.Fe Fe Fe O2 O2 |
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
则有关该电池的说法正确的是
| A.充电时阳极反应:Ni(OH)2-e—+OH-=NiOOH+H2O |
| B.充电过程是化学能转化为电能的过程 |
| C.放电时负极附近溶液的碱性不变 |
| D.放电时电解质溶液中的OH- 向正极移动 |
下列离子方程式书写正确的是
| A.Na2O2投入水中:2Na2O2+2H2O = 4Na++4OH−+ H2↑ |
| B.向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O = HClO+HSO3- |
| C.钠投入CuSO4溶液中:2Na+Cu2++2H2O = 2Na++Cu(OH)2↓+H2↑ |
| D.铜和稀HNO3反应:3Cu+8H++2NO3-= 3Cu2++2NO2↑+4H2O |
下列操作中,完全正确的一组是
①用试管夹夹持试管时,试管夹从试管底部往上套,夹在试管的中上部
②给盛有液体的体积超过1/3容积的试管加热
③把鼻孔靠近容器口去闻气体的气味
④将试管平放,用纸槽往试管里送入固体粉末后,然后竖立试管
⑤取用放在细口瓶中的液体时,取下瓶塞倒放在桌面上,倾倒液体时,瓶上的标签对着地面
⑥将烧瓶放在桌上,用力塞紧塞子
⑦用坩埚钳夹取加热后的蒸发皿
⑧将滴管垂直伸进试管内滴加液体
⑨稀释浓硫酸时,把水迅速倒入盛有浓硫酸的量筒中
⑩检验装置的气密性时,把导管的一端浸入水中,用手捂住容器的外壁或用酒精灯微热
| A.①④⑦⑩ | B.①④⑤⑦⑩ | C.①④⑤⑦⑧⑩ | D.④⑤⑦⑩ |
设NA为阿伏伽德罗常数的值,下列叙述正确的是
| A.100 mL 2.0 mol·L-1 NH4Cl溶液中含有NH4+ 的数目为0.2NA |
| B.25℃时,pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA |
| C.标准状况下,2.24L庚烷含有的分子数为0.1NA |
| D.常温常压下,NO2与足量H2O反应生成0.1molNO,则转移的电子数为0.2NA |
某无色透明溶液中可能含有以下离子中的若干种K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、CO32-、I-和Cl-,取该溶液进行如下实验:
①溶液滴在pH试纸上,呈红色
②将少许溶液加入铜片和硫酸,有无色气体产生,此气体与空气混合,立即变成红棕色
③取少许溶液滴入BaCl2溶液,则产生白色沉淀
④取实验③中的澄清溶液,滴入AgNO3溶液,产生不溶于稀HNO3的白色沉淀
⑤另取少许溶液,滴入NaOH溶液,有白色沉淀生成,当NaOH过量时,又有部分白色
沉淀溶解。根据以上现象判断原溶液中:
| A.②中无色气体中有NO,可能含CO2 |
| B.③中沉淀有BaSO4,可能含BaCO3 |
| C.肯定存在的离子是Al3+、SO42-、NO3-、Mg2+,肯定不存在的离子是Ba2+、Fe2+、CO32-、I-,不能确定的离子是K+ 、Cl- |
| D.②中红棕色气体通入水中发生反应的离子方程式为:3NO2 + H2O = H++ NO3- + 2NO |