一般情况下,胶体粒子不易聚集而稳定,主要是因为( )
| A.胶体有丁达尔效应 |
| B.胶体有布朗运动 |
| C.胶粒很小,不受重力作用 |
| D.同种胶粒带同种电荷,它们互相排斥 |
下列事实,不能用勒夏特列原理解释的是
| A.新制的氯水在光照下颜色变浅 |
| B.H2、I2、HI平衡混合气加压后颜色变深 |
| C.合成 NH3反应,为提高 NH3的产率,理论上应采取相对较低温度的措施 |
| D.实验室用排饱和食盐水而不用排水法收集氯气 |
用惰性材料作电极,分别电解下列物质,当相同电量时,下列指定的电极上析出气体质量最大的是
| A.熔融的NaCl(阳极) | B.NaCl溶液(阴极) |
| C.NaOH溶液(阴极) | D.Na2SO4(阳极) |
下列关于化学能与电能相互转化的说法正确的是
| A.在原电池中,化学能转变为电能,电子沿导线由正极流向负极 |
| B.双液原电池通过盐桥连接,KCl盐桥中K+朝正极定向迁移 |
| C.在电解池中,与电源负极相连的电极称为阳极,溶液中阴离子朝阳极定向迁移 |
| D.电解氯化铜溶液,在阴极上产生的气体能使湿润的KI-淀粉试纸变蓝 |
已知448℃时反应H2(g)+I2(g) 2HI(g)的平衡常数是49,则HI(g)
2HI(g)的平衡常数是49,则HI(g)
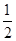 H2(g)+
H2(g)+ 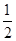 I2(g) 在该温度下的平衡常数是
I2(g) 在该温度下的平衡常数是
A. |
B.2401 | C.7 | D.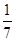 |
汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2+Pb+2H2SO4=2PbSO4+2H2O,根据此反应判断下列叙述中正确的是
| A.PbO2是电池的负极 |
| B.负极的电极反应式为:Pb+SO42--2e–=PbSO4 |
| C.PbO2得电子,被氧化 |
| D.电池放电时,溶液酸性增强 |