某空气污染监测仪是根据SO2和Br2的定量反应来测定空气中SO2含量的。参加反应的溴,来自一个装满酸性(H2SO4)KBr溶液的电解槽阳极上的氧化反应,电解槽的阳极室与阴极室是隔开的。当测量某地区空气中SO2含量时,空气(经过除尘)以1.5×10-4 m3·min-1的流速进入电解槽的阳极室,电流计显示每分钟通过电子是5.136×10-9 mol,此条件下能保持溴浓度恒定并恰好与SO2完全反应。设被测空气中不含其他能与溴反应的杂质。
(1)写出此监测过程中发生的主要反应的化学方程式。
(2)计算该地区空气中SO2的含量(g·m-3)(保留两位小数)。
(8分)将0.2molMg、Al的混合物用盐酸完全溶解,放出标准状况下5.6L气体,然后再滴入2mol/LNaOH溶液,请回答:(写计算过程)
(1)若该Mg、Al的混合物与盐酸恰好完全反应,在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积是多少?
(2)若该Mg、Al混合物溶于200ml 3mol/L盐酸后,滴入NaOH溶液,使所得沉淀中无Al(OH)3,则滴入NaOH溶液的体积最少为多少?
5.3g Na2CO3正好与20mL盐酸完全反应生成二氧化碳。问这种盐酸的物质的量浓度为多少?产生的CO2在标准状况下的体积是多少?
常温下将20.0 g14%的NaCl溶液跟30 g24%的NaCl溶液混合,得到密度为1.15 g/mL的混合溶液,计算:
①该混合溶液的质量分数。
②该混合溶液的物质的量浓度。
③1000g水中需加多少物质的量的NaCl,才能使浓度恰好与上述混合液的浓度相等?
将某种碳酸钠晶体(Na2CO3 · nH2O)和碳酸氢钠的混合物11.24 g,加热到质量不再减少,剩余残渣8.48 g。加热时产生的气体依次通过浓H2SO4和NaOH溶液后,NaOH溶液增重1.32 g(假设气体全部被吸收)。试计算:
(1)求n的值
(2)求混合物中碳酸钠晶体与碳酸氢钠的物质的量。
已知850℃时,CO(g)+H2O(g)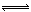 CO2(g)+H2(g)的K=1。850℃时,若在容积为2L的密闭容器中同时充入1.0mol CO,3.0mol H2O,1.0mol CO2和xmol H2。
CO2(g)+H2(g)的K=1。850℃时,若在容积为2L的密闭容器中同时充入1.0mol CO,3.0mol H2O,1.0mol CO2和xmol H2。
(1)当x=5.0时,判断化学反应进行的方向。
(2)若要使上述反应开始时向正反应方向进行,则x应满足的条件是什么?
(3)若x=5.0,当上述反应达到平衡后,计算H2的体积分数。