(7分)某化学反应2A B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20 min内平均速率为__________mol·L-1·min-1。
(2)在实验2,A的初始浓度为c2="__________" mol·L-1,反应经20 min就达到平衡,可推测实验2中还隐含的条件是_______________________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3__________v1(填>、=或<),且c3__________1.0 mol·L-1(填>、=或<)。
(4)比较实验4和实验1,可推测该反应是__________反应(选填“吸热”或“放热”),理由是_____________________________________________________________________。
由铜片、锌片和200mL稀硫酸组成的原电池中,当铜片上放出3.36L(标状况)气体时(锌片上无气体产生),硫酸恰好反应完.计算:
(1)产生这些气体消耗的金属是哪一种,消耗的质量是多少;
(2)有多少电子通过了导线;
(3)硫酸溶液的物质的量浓度是多少.
将Cu与CuO的混合物20.8g加入到50mL 18.4mol/L浓H2SO4中,加热充分反应至固体物质完全溶解,冷却后将混合液稀释至1000 mL,测得c(Cu2+ )="0.3" mol/L。试计算:(本题无计算过程不给分)
)="0.3" mol/L。试计算:(本题无计算过程不给分)
(1)反应过程中放出的 气体在标准状况下的体积(不考虑气体在溶液中的溶解)。
气体在标准状况下的体积(不考虑气体在溶液中的溶解)。
(2)溶液稀释后,c(H+)是多少?
元素R的气态氢化物化学式为HxR.在标准状况下,8.5gHxR气体的体积是5.6L。将5. 1gHxR气体通入200ml 0.75mol/L的CuCl2溶液中正好完全反应,并生成黑色沉淀。
( 1)HxR的相对分子质量为;
1)HxR的相对分子质量为;
(2)x等于,R元素的名称为。
(3)反应的化学方程式为
由铜片、锌片和200mL稀硫酸组成的原电池中,当铜片上放出3.36L(标状况)气体时(锌片上无气体产生),硫酸恰好反应完.计算:
(1)产生这些气体消耗的金属是哪一种,消耗的质量是多少;
(2)有多少电子通过了导线;
(3)硫酸溶液的物质的量浓度是多少.
下图是研究甲烷取代反应实验装置图,具体的实验方法是:
取一个100 mL的大量筒,用排饱和食盐水的方法先后收集20 mL C H4和80 mL Cl2,进行实验。
H4和80 mL Cl2,进行实验。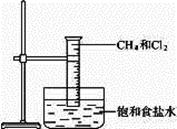
(1)若研究甲烷与氯气的取代反应,还需要的条件是________________________________。
(2)若将如图所示装置放在光亮的地方,等待片刻,观察到的现象是__________________。
(3)若将如图所示装置放在强光下照射会有_________________(填可能发生的不良后果)。
(4)写出甲烷和氯气的第一步反应方程式。
A和B反应生成C,假定反应由A、B开始,它们的起始浓度均为1mol/L。反应进行2min后A的浓度为0.8mol/L,B的浓度为0.6mol/L。求2min内A B 反应的平均速率。