β′Al2O3陶瓷作固体电解质,反应式如下:2Na+xS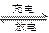 Na2Sx,以下说法正确的是
Na2Sx,以下说法正确的是
| A.放电时,Na作正极,S极发生还原反应 |
| B.若用此电池电解硝酸银溶液,当阴极上产生标准状况下气体1.12 L时,消耗金属钠2.3 g |
| C.充电时,钠极与外电源的正极相连 |
D.充电时,阳极发生的反应为  xS+2e- xS+2e- |
下列大小顺序排列完全正确的组合是
| A.气态氢化物的稳定性:HF>NH3>PH3>H2S |
| B.沸点:苯酚>CH3OH>HCHO>CH3COOH |
| C.离子半径:S2->O2->F- |
| D.相同温度、相同浓度溶液中水的电离程度:NH4Cl>CH3COOH>HCl>Ba(OH)2 |
某溶液灼烧时,透过蓝色钴玻璃未见到紫色火焰,下列判断中错误的是
| A.该溶液中一定不含钾元素 | B.该溶液中不可能含钠的化合物 |
| C.该溶液中不可能含钠单质 | D.该溶液中可能含钠的化合物 |
下列物质的化学用语正确的是
A.二氧化碳的电子式: |
B.次氯酸的结构式:H—Cl—O |
C.甲烷分子的球棍模型: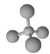 |
D.S2-的离子结构示意图: |
美国科学家理查德·赫克(Richard F, Heck)和日本科学家根岸英一(Ei-ichi Negishi) 、铃木章(Akira Suzuki)因在有机合成领域中钯催化交叉偶联反应方面的卓越研究获诺贝尔化学奖。这一成果广泛应用于制药、电子工业和先进材料等领域,为化学家们提供“精致工具”,大大提升合成复杂化学物质的可能性。下列有关催化剂的表述错误的是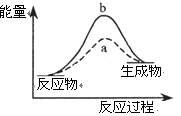
| A.催化剂是改变化学反应速率最有效的手段之一 |
| B.催化剂自身的组成、化学性质和质量在反应前后不发生变化 |
| C.同一反应可以有不同的催化剂,同一催化剂也可用于不同的反应 |
| D.上图中b表示使用催化剂的情况,a表示无催化剂的情况 |
下列说法正确的是
| A.道尔顿、汤姆生、卢瑟福和门捷列夫等科学家对原子结构模型的建立均作出了卓越的贡献 |
| B.神七宇航员所穿出仓航天服是由我国自行研制的新型“连续纤维增韧”航空材料做成,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料 |
| C.淀粉、纤维素互为同分异构体,都属于糖类;硝酸纤维、铜氨纤维都属于酯类 |
| D.生物质能来源于植物及其加工产品所贮存的能量,但不包括城市与工业有机废弃物和农业废弃物等 |