1996年诺贝尔化学奖授予对发现C60有重大贡献的三位科学家。C60分子是形如球状的多面体,如右图,该结构的建立基于以下考虑:C60分子中每个碳原子只跟相邻的3个碳原子形成化学键;C60分子只含有五边形和六边形;碳与碳之间既有单键又有双键,每个碳原子仍然满足四个价键饱和;多面体的顶点数、面数和棱边数的关系,遵循欧拉定理:顶点数+面数-棱边数=2。
请完成下列问题:
(1)一个C60分子中有多少个五边形和多少个六边形?
(2)一个C60分子中有多少个C=C?
(3)已知C70分子的结构模型也遵循C60的那些规律,请确定C70分子结构中上述几项参数。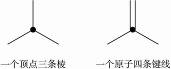
如图所示,室温下向盛有3.0mLNO的试管中缓缓通入1.5mLO2(所有气体均在标准状况下测定)。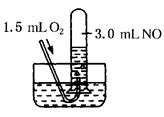
试回答下列问题:
(1)写出观察到的现象(可不写满,也可补充):
①___________________________________________________;
②___________________________________________________;
③___________________________________________________。
(2)最终试管中剩余的气体是________,体积为______。
将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。请回答:
(1)NO的体积为________L,NO2的体积为________L。
(2)待产生的气体全部释放后,向溶液中加入VmLamol/L的NaOH溶液,恰好使溶液中Cu2+全部转化成沉淀,则原硝酸溶液的浓度为__________mol/L。
、现有Na2CO3、NaHCO3、NaOH的固体混合物共27.2g,将固体完全溶于水配成溶液后,向该溶液中逐滴加入1mol/L的盐酸。所加入盐酸溶液的体积与产生的CO2气体体积的关系如图所示: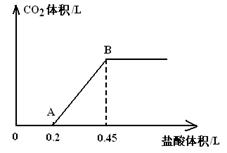
(1)写出OA段所发生反应的离子方程式;
(2)B点所产生的CO2的体积是_____________L(标准状况);
(3)原混合物中NaOH的质量为_____________g。
、0.6mol·L-1Fe2(SO4)3和1.2mol·L-1CuSO4的混合溶液200mL,加入一定量铁粉充分反应后,测得溶液中Fe2+与Cu2+物质的量之比为2:1,则加入铁粉的物质的量是多少摩尔?
有Na2SO4和Na2CO3混合溶液10.0毫升,加入足量BaCl2溶液,充分反应后,经过滤、洗涤和烘干,得到白色沉淀1.451克。将沉淀与过量盐酸反应,得到112毫升CO2气体(标准状况)。求原混合溶液中Na2SO4和Na2CO3的物质的量浓度(写出计算过程)。