下列关于晶体的说法一定正确的是( )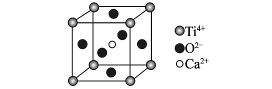
CaTiO3的晶体结构模型(图中Ca2+、O2-、
Ti4+分别位于立方体的体心、面心和顶点)
| A.分子晶体中都存在共价键 |
| B.CaTiO3晶体中每个Ti4+与12个O2-相邻 |
| C.SiO2晶体中每个硅原子与两个氢原子以共价键相结合 |
| D.金属晶体的熔点都比分子晶体的熔点高 |
石灰石在自然界中存量丰富,它是许多工业的主要原料之一。但制取下列物质不需要石灰石的是()
| A.制玻璃 | B.制陶瓷 | C.制水泥 | D.制漂粉精 |
下列有关环境保护的说法中错误的是()
| A.含氮、磷化合物的生活污水大量排放可使水体富营养化,使自然水域产生“水华”现象 |
| B.为防止全球气候变暖的进一步恶化,联合国环保组织要求各国大量减少二氧化硫的工业排放量 |
| C.甲醛、苯及其同系物、氨气、氡气等是劣质建筑材料和装修材料释放出的常见污染物,对人体有害 |
| D.废旧电池的集中处理是为了防止其中的重金属离子对土壤和水源造成污染 |
下列原料或制成的产品中,若出现破损不可以进行热修补的是()
| A.聚氯乙烯凉鞋 | B.电木插座 |
| C.自行车内胎 | D.聚乙烯塑料膜 |
采用循环操作可提高原料的利用率,在下列工业生产中,没有采用循环操作的是()
| A.硫酸 | B.合成氨 | C.硝酸 | D.氯碱 |
下列说法正确的是()
| A.煤、石油、天然气是当今世界上最重要的三大矿物燃料,是取之不尽的 |
| B.煤是由无机物和有机物所组成的复杂的混合物,主要含有碳和氢两种元素 |
| C.石油主要含有碳和氢两种元素,同时还含有少量的硫、氧、氮等元素 |
| D.煤和石油都是由古代植物遗体埋在地层下或在地壳中经过一系列非常复杂的变化而形成的 |