下列各项叙述正确的是( )
| A.在氯化钠晶体中,只有阴离子和阳离子,没有NaCl分子 |
| B.在氯化钠晶体中存在NaCl分子 |
| C.石英是由SiO2形成的分子晶体 |
| D.金刚石和石墨晶体都是由碳原子网状结构形成的典型的原子晶体 |
一定温度下,将1molA(g)和1molB(g)充入2L密闭容器中发生反应,在 时达平衡:
时达平衡: 时刻分别改变反应的一个条件,测得溶器中C(g)的浓度随时间变化如图所示。有关说法正确的是
时刻分别改变反应的一个条件,测得溶器中C(g)的浓度随时间变化如图所示。有关说法正确的是
A. 间该反应的平衡常数相同,均为0.25 间该反应的平衡常数相同,均为0.25 |
B. 时刻改变的条件是使用催化剂 时刻改变的条件是使用催化剂 |
C. 时刻改变的条件是移去少量D 时刻改变的条件是移去少量D |
| D.反应方程式中x=2 |
下图表示反应 ,在不同条件下反应混合物中C的百分含量反应过程所需时间的关系曲线。下列有关叙述正确的是
,在不同条件下反应混合物中C的百分含量反应过程所需时间的关系曲线。下列有关叙述正确的是
| A.反应由逆反应开始 |
| B.a表示有催化剂,b表示无催化剂 |
| C.若n=2,其它条件相同,a比b的压强大 |
| D.若其它条件相同,a比b的温度高 |
常温下,pH=12的氢氧化钠溶液pH=4的醋酸溶液等体积混合后恰好中和,忽略混合后溶液体积的变化,下列说法中正确的是
| A.混合前的醋酸约1%发生电离 | B.混合后的溶液中 |
| C.氢氧化钠和醋酸和浓度不相等 | D.混合后的溶液呈中性 |
三氟化氮 是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生如下反应:
是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生如下反应: 。下列有关该反应的说法正确的是
。下列有关该反应的说法正确的是
A. 是还原剂 是还原剂 |
B. 非极性分子,在潮湿空气中泄漏会看到红棕色气体 非极性分子,在潮湿空气中泄漏会看到红棕色气体 |
| C.每消耗0.2mol氧化剂,可收集到5.418L气体 |
D.若生成1mol  个电子 个电子 |
甲酸为一元弱酸,在15mL0.1mol/L KOH溶液中逐滴加入0.2mol/L甲酸溶液,溶液的pH变化和所加入的甲酸的体积关系描绘成如图所示曲线。下面有关微粒浓度的大小关系正确的是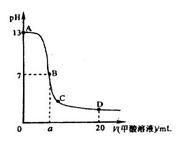
A.在A、B间的任意一点上都存在:


B.在B点:
 ,且a=7.5
,且a=7.5
C.在C点: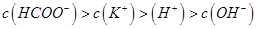
D.在D点: