不能用离子方程式: +2H+====CO2↑+H2O来表示的反应是
+2H+====CO2↑+H2O来表示的反应是
| A.碳酸钡和盐酸 |
| B.碳酸氢钾和H2SO4 |
| C.碳酸钠与硝酸 |
| D.碳酸铵与盐酸 |
下列各组物质中,满足右图物质一步转化关系的选项是()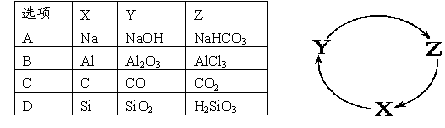
下列各组物质的性质比较,不正确的是()
| A.酸性:HClO4>H2SO4>H3PO4 | B.氢化物稳定性:H2S>HF>H2O |
| C.碱性:NaOH>Mg(OH)2>Al(OH)3 | D.氧化性:F2>Cl2>Br2>I2 |
下列表示物质结构的化学用语或模型中,正确的是()
A.HF的电子式: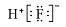 |
B.Cl-离子的结构示意图: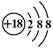 |
C.8个中子的碳原子的核素符号: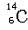 |
D.CH4分子的球棍模型: |
化学与生产、生活、社会密切相关。下列有关说法中,错误的是()
| A.今夏,温州地区出现了严重的旱情,缓解旱情的措施之一是用碘化银进行人工增雨 |
| B.新能源汽车的推广与使用有助于减少光化学烟雾的产生 |
| C.利用太阳能、风能和氢能等能源替代化石能源有利于实现“低碳经济” |
| D.华裔科学家高琨在光纤传输信息领域中取得突破性成就,光纤的主要成分是高纯度的单质硅 |
9.7 g Cu和Zn的合金与足量的稀HNO3反应,还原产物只有NO气体,其体积在标准状况下为2.24 L,将溶液稀释为1 L,测得溶液的pH=1,此时溶液中NO3-的浓度为()
| A.0.3 mol/L | B.0.4 mol/L | C.0.5 mol/L | D.0.6 mol/L |