在标准状况下,1 L水中溶解700 L NH3,所得溶液的密度为0.9 g·cm-3,则氨水的浓度为
| A.18.4 mol·L-1 | B.20.4 mol·L-1 | C.37.7% | D.38.5% |
对于合成氨反应,达到平衡后,以下分析正确的是( )
| A.升高温度,对正反应的反应速率影响更大 |
| B.增大压强,对正反应的反应速率影响更大 |
| C.减小反应物浓度,对逆反应的反应速率影响更大 |
| D.加入催化剂,对逆反应的反应速率影响更大 |
某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质) 制取七水合硫酸亚铁(FeSO4·7H2O) ,设计了如下流程: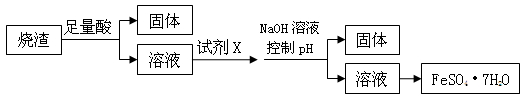
下列说法不正确的是 ( )
| A.溶解烧渣选用足量硫酸,试剂X选用铁粉 |
| B.固体1中一定含有SiO2,控制pH是为了使Al3+转化为Al(OH)3,进入固体2 |
| C.从溶液2得到FeSO4·7H2O产品的过程中,须控制条件防止其氧化和分解 |
| D.若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4·7H2O |
某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是( )
| A.甲装置:可用来证明碳的非金属性比硅强 |
| B.乙装置:橡皮管的作用是能使水顺利流下 |
| C.丙装置:用图示的方法不能检查此装置的气密性 |
| D.丁装置:先从①口进气集满二氧化碳,再从②口进气,可收集氢气 |
a molNa2O2和b molNaHCO3固体混合后,在密闭容器中加热到250℃,使其充分反应,当排出气体为两种气体时, a:b不可能为
| A.3:4 | B.4:5 | C.2:3 | D.3:2 |
如图是第三周期11~17号元素某些性质变化趋势的柱形图,下列有关说法中正确的是( )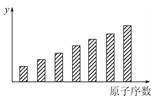
| A.y轴表示的可能是基态的原子失去一个电子所需要的最小能量; |
| B.y轴表示的可能是原子在化合物中吸引电子的能力标度; |
| C.y轴表示的可能是原子半径; |
| D.y轴表示的可能是形成基态离子转移的电子数 |