甲烷与过量氧气混合,用电火花引爆后,测得爆炸后的气体密度为同温、同压下氢气密度的14倍,则原混合气体中氧气与甲烷的体积比为( )
| A.1∶5 | B.1∶3 | C.3∶1 | D.3∶2 |
一定温度下的反应A(g)+3B(g) 2C(g),下列叙述不能表明它达到化学平衡的是
2C(g),下列叙述不能表明它达到化学平衡的是
A.A、B、C的浓度不再变化
B.混合气体的总物质的量不再变化
C.单位时间内生成a mol A,同时生成3amol B
D.C的生成速率与C的分解速率相等
高温下,某反应达平衡,平衡常数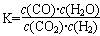 。恒容时,温度升高,H2浓度减小。下列说法正确的是
。恒容时,温度升高,H2浓度减小。下列说法正确的是
| A.该反应的焓变为正值 |
| B.恒温恒容下,增大压强,H2浓度一定减小 |
| C.升高温度,逆反应速率减小 |
D.该反应化学方程式为CO + H2 O CO2+ H2 CO2+ H2 |
关于下列四个图像的说法中不正确的是
A.图①表示可逆反应: CO(g) + H2O(g) CO2(g)+ H2(g) ΔH<0 CO2(g)+ H2(g) ΔH<0 |
| B.图②表示电解氯化钠的稀溶液,阴、阳两极产生气体体积之比一定是1∶1 |
C.图③表示可逆反应:A2(g)+ 3B2(g) 2AB3(g)ΔH >0 2AB3(g)ΔH >0 |
D.图④表示压强对可逆反应2A(g)+ 2B(g) 3C(g)+ D(s)的影响,乙的压强大 3C(g)+ D(s)的影响,乙的压强大 |
根据右表提供的数据,判断在等物质的量浓度的NaClO
和NaHCO3混合溶液中,各种离子浓度关系正确的是
| A.c(Na+)>c(HCO3-)+c(ClO-)+2c(CO32-) |
| B.c(ClO-)>c(HCO3-)>c(H+) |
| C.c(HClO)+c(ClO-)=c(HCO3-)+c(CO32-)+c(H2CO3) |
| D.c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+c(OH-) |
设nA 代表阿伏加德罗常数(NA )的数值,下列说法正确的是
| A.1 mol 硫酸钾中阴离子所带电荷数为nA |
| B.乙烯和环丙烷(C3H6)组成的28g混合气体中含有3nA 个氢原子 |
| C.标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为nA |
| D.将0.1mol氯化铁溶于1L水中,所得溶液含有0.1nA个Fe3+ |