下列离子方程式书写正确的是 ( )
| A.FeCl2溶液中通Cl2:Fe2++Cl2===Fe3++2Cl- |
B.澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO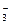 ===CaCO3↓+H2O ===CaCO3↓+H2O |
| C.FeS固体放入稀硝酸溶液中:FeS+2H+===Fe3++H2S↑ |
| D.AlCl3溶液中加入过量氨水:Al3++4OH-===AlO2-+2H2O |
实验是研究化学的基础,下图中所示的实验方法、装置或操作完全正确的
| A.干燥Cl2 | B.吸收HCl |
| C.制取Fe(OH)2沉淀 | D.稀释浓H2SO4 |
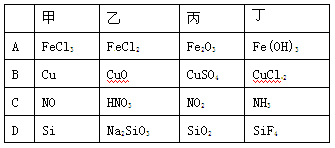
下列各组物质按下图所示转化关系每一步都能一步实现的是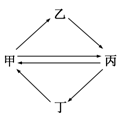
下列说法正确的是
| A.HClO中氯元素化合价比HClO4中氯元素化合价低,所以,HClO4的氧化性强 |
| B.已知①Fe + Cu2+ = Fe2+ + Cu;② 2Fe3+ + Cu = 2Fe2+ + Cu2+,则氧化性强弱顺序为:Fe3+ > Cu2+> Fe2+ |
| C.已知还原性:B-> C-> D-,反应 2C-+ D2 = 2D-+C2和反应 2C-+ B2=2B-+C2都能发生 |
| D.具有强氧化性和强还原性的物质放在一起就能发生氧化还原反应 |
下列叙述正确的是
①久置于空气中的氢氧化钠溶液,加盐酸时有气体产生
②浓硫酸可用于干燥H2、SO2等气体,但不能干燥NH3、NO2等气体
③Na2O2与CO2反应生成Na2CO3和O2,SO2和Na2O2反应生成Na2SO3和O2
④足量的硫单质与64g铜反应,有2mol电子发生转移
⑤蔗糖炭化的演示实验中,浓硫酸既体现了其强氧化性又体现了其脱水性
⑥氢氧化铁胶体与氯化铁溶液分别蒸干灼烧得相同的物质
| A.①④⑤ | B.①⑤⑥ | C.②③④ | D.④⑤⑥ |
设NA表示阿伏伽德罗常数,下列说法中不正确的是
| A.一定量的Fe与含1molHNO3的稀硝酸恰好反应,则被还原的氮原子数小于NA |
| B.1molFeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒 |
| C.0.01molMg在空气中完全燃烧生成MgO和Mg3N2,转移电子数目为0.02NA |
| D.125gCuSO4•5H2O晶体中含有0.5NA个Cu2+ |