某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
(一)制取氧化铜
①称取2 g CuSO4·5H2O研细后倒入烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是__________(填实验序号),步骤①③中研磨固体所用仪器的名称是__________;
(2)步骤③中洗涤沉淀的操作是________________________________________。
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较
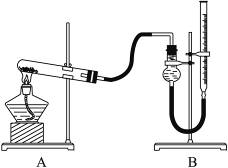
用下图所示装置进行实验,实验时均以生成25 mL气体为准,其他可能影响实验的因素均已忽略,相关数据见下表:
| 实验序号 |
KClO3质量 |
其他物质质量 |
待测数据 |
| ④ |
1.2 g |
无其他物质 |
|
| ⑤ |
1.2 g |
CuO 0.5 g |
|
| ⑥ |
1.2 g |
MnO2 0.5 g |
|
回答下列问题:
(3)上述实验中的“待测数据”指__________;
(4)本实验装置图中量气装置B由干燥管、乳胶管和50 mL滴定管改造后组装而成,此处所用滴定管是__________(填“酸式”或“碱式”)滴定管;
(5)若要证明实验⑤中干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上的单孔橡皮塞,____________________;
(6)为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作步骤):
a.__________________________________________________;
b.证明CuO的化学性质有没有改变。
质量相等的SO2和SO3,所含氧原子数之比为
| A.1:1 | B.2:3 | C.6:5 | D.5:6 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.含有NA个氦原子的氦气在标准状况下的体积约为11.2L |
| B.25℃,1.01×105 Pa, 32 g O2和O3的混合气体所含原子数为2NA |
| C.标准状况下,11.2LH2O 含有的分子数为0.5NA |
| D.在常温常压下,44gCO2含有的分子数为3NA |
某溶液中只含有Na+、Al3+、Cl-、SO42-四种离子,已知前三种离子的个数比为3∶2∶1,则溶液中Al3+和 SO42-的离子个数比为
| A.1∶4 | B.1∶2 | C.3∶4 | D.3∶2 |
下列各组仪器:①漏斗;②容量瓶;③广口瓶;④分液漏斗;⑤天平;⑥量筒;⑦胶头滴管;
⑧蒸馏烧瓶。常用于物质分离的是
| A.①③⑦ | B.②⑥⑦ | C.①④⑧ | D.④⑥⑧ |
X、Y、Z、W各代表一种物质,若X+Y===Z+W,则X和Y之间不可能是
| A.盐和盐的反应 |
| B.碱性氧化物和水的反应 |
| C.酸与碱的反应 |
| D.酸性氧化物和碱的反应 |