下列对实验现象的解释与结论正确的是
| 编号 |
实验操作 |
实验现象 |
解释与结论 |
| A |
向鸡蛋清溶液中加入饱和(NH4)2SO4溶液 |
有白色沉淀产生 |
蛋白质发生了变性 |
| B |
向某溶液中加入BaCl2溶液 |
有白色沉淀产生 |
生成难溶于水的BaSO4,该溶液中一定含有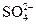 |
| C |
向甲苯中滴入少量浓溴水,振荡,静置 |
溶液分层,上层呈橙红色,下层几乎无色 |
甲苯和溴水发生取代反应,使溴水褪色 |
| D |
向蔗糖中加入浓硫酸 |
变黑,放热,体积膨胀,放出刺激性气体 |
浓硫酸具有脱水性和强氧化性,反应中生成C、SO2和CO2等 |
下列各组物质熔化或气化时,所克服的粒子间作用属于同种类型的是( )
| A.C60和SiO2熔化 | B.Mg和S熔化 |
| C.氯酸钾和蔗糖熔化 | D.碘和干冰升华 |
下列各组物质各自形成的晶体,均属于分子晶体的化合物是( )
A. NH3、HD、C10H8 B.PCl3、CO2、CH3COONH4
C. NO、SiO2、P2O5 D.H2O2、CF2Cl2、B3N3H6
关于晶体的下列说法正确的是( )
| A.在晶体中只要有阳离子就一定要有阴离子 |
| B.在晶体中只要有阴离子就一定要有阳离子 |
| C.原子晶体的熔点一定比金属晶体的高 |
| D.分子晶体的熔点一定比金属晶体的低 |
下列各组物质中,按熔点由低到高排列的是( )
| A.O2、I2、Hg | B.CO2、KCl、SiO2 | C.Na、K、Rb | D.NaCl、KCl、RbCl |
向盛有少量NaCl溶液的试管中滴入少量AgNO3溶液,再加入氨水,下列关于实验现象的叙述不正确的是( )
| A.先生成白色沉淀,加入足量氨水后沉淀消失 |
| B.生成的沉淀为AgCl,它不溶于水,但溶于氨水,重新电离成Ag+和Cl- |
| C.生成的沉淀是AgCl,加入氨水后生成了可溶性的配合物[Ag(NH3)2]Cl |
| D.若向AgNO3溶液中直接滴加氨水,产生的现象也是先出现白色沉淀后沉淀消失 |